题目内容
一定量的Fe2(SO4)3溶液在煮沸条件下被25.0 mL 0.049 mol·L-1羟氨(NH2OH)的酸性溶液还原成Fe2+,生成的Fe2+与22.50 mL 0.020 mol·L-1的KMnO4溶液恰好完全反应:Fe2++MnOA.N2
B.N2O
C.NO
D.NO2
解析:根据化合价升降总数相等,可求得N在氧化产物中的化合价为+2。
答案:B

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
已知Fe3+的氧化性强于I2,某澄清溶液中可能只含有Na+、Fe3+、Fe2+、SO
、Cl-、Br-、I-中的若干种,现取部分溶液依次进行如下实验:
①通入一定量Cl2后,加入CCl振荡,静置后CCl层呈紫红色,用分液漏斗分液;
②向分液后的水溶液中加入足量硝酸酸化的硝酸钡溶液,产生白色沉淀;
③过滤后将滤液分为两份,向一份中加入硝酸酸化的硝酸银溶液,产生大量沉淀,向另一份中加入少量KSCN溶液,溶液立即变为血红色.
根据上述实验,以下推测正确的是( )
2- 4 |
①通入一定量Cl2后,加入CCl振荡,静置后CCl层呈紫红色,用分液漏斗分液;
②向分液后的水溶液中加入足量硝酸酸化的硝酸钡溶液,产生白色沉淀;
③过滤后将滤液分为两份,向一份中加入硝酸酸化的硝酸银溶液,产生大量沉淀,向另一份中加入少量KSCN溶液,溶液立即变为血红色.
根据上述实验,以下推测正确的是( )
| A、无法确定原溶液中是否存在Cl-、Na+? | ||
B、原溶液中肯定存在的离子有Fe3+、SO
| ||
| C、原溶液一定显中性 | ||
| D、原溶液中肯定不存在的离子有Fe2+、Br- |
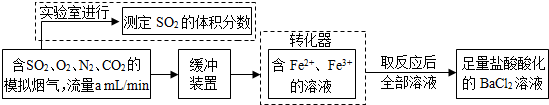
在实验室中,为验证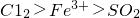 的氧化性顺序,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已省略,气密性已经检验).
的氧化性顺序,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已省略,气密性已经检验).
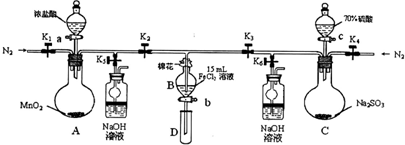
(1)打开K1~K4,关闭K5、K6,通入一段时间N2,目的是______.
(2)关闭K1、K3、K4,打开活塞a,滴加一定量的浓盐酸,给A加热,A中发生反应的离子方程式为______.
(3)当B中的溶液变黄时,停止加热,夹紧弹簧夹K2并打开K5,这样做的原因是______.
(4)打开活塞b,使约2mL的溶液流入试管D中,滴入______可以证明其中是否含有Fe3+离子.
(5)打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3并打开K6,用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是______.
(6)更新试管D,打开活塞b,使约2mL的溶液流入试管D中,检验B溶液中的离子.检验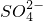 所需的试剂是______.
所需的试剂是______.
A.Ba(NO3)2溶液 B.BaC12溶液 C.AgNO3溶液 D.Ba(OH)2溶液
甲、乙、丙三位同学分别对两次B中得到的溶液进行了有关离子的检测,他们的检测结果一定能够证明氧化性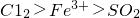 的是______.
的是______.
| 第一次B中溶液含有离子 | 第二次B中溶液含有离子 | |
| 甲 | 有Fe2+,无Fe3+ | 有SO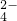 |
| 乙 | 既有Fe3+,又有Fe2+ | 有SO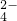 |
| 丙 | 有Fe3+,无Fe2+ | 有Fe2+ |


 、Cl-、Br-、I-中的若干种,现取部分溶液依次进行如下实验:
、Cl-、Br-、I-中的若干种,现取部分溶液依次进行如下实验: