题目内容
我国地质学家发现一种化学式为Ca3Li2(BeSiO4)3F2的矿石.下列说法正确的是( )
| A、该矿石所含非金属元素的简单氢化物中,SiH4的沸点最高 |
| B、该矿石所含金属元素中,Be的原子半径最小 |
| C、该矿石所含金属元素都是+2价 |
| D、该矿石中所含元素都是短周期元素 |
考点:含硅矿物及材料的应用
专题:元素及其化合物
分析:A.该矿石所含非金属元素为:Si、O、F,利用相对分子质量分析分子间作用力,并注意氟化氢、水分子中有氢键分析解答;
B.香花石中处于同一周期的四种元素为Li、Be、O、F,同主族自左而右原子半径减小,金属元素为Ca、Li、Be;
C.该矿石所含金属元素Li+1价,据此分析解答;
D.短周期元素是指第一至第三周期的前18种元素;
B.香花石中处于同一周期的四种元素为Li、Be、O、F,同主族自左而右原子半径减小,金属元素为Ca、Li、Be;
C.该矿石所含金属元素Li+1价,据此分析解答;
D.短周期元素是指第一至第三周期的前18种元素;
解答:
解:A.结构相似,相对分子质量越大,分子间作用力越大,沸点越高.SiH4相对分子质量最大,因此氟化氢、水的沸点低于SiH4,但氟化氢、水分子间还存在氢键,则氟化氢、水的沸点高于SiH4,氟化氢常温下为气态、水常温下为液态,水的沸点最高,故A错误;
B.香花石中,Ca的电子层数大于Li、Be、O、F,Li、Be、O、F为处于同一周期的四种元素,同主族自左而右原子半径减小,非金属性增强,故原子半径Ca>Li>Be>O>F,所含金属元素中,Be的原子半径最小,故B正确;
C.该矿石中化合价分别为:Ca+2价,Be+2价,Si+4价,O-2价,F-1价,则根据化合价的原则(在化合物中正、负化合价的代数和为零),设Li元素的化合价为x,(+2)×3+x×2+[(+2)+(+4)+(-2)×4]×3+(-1)×2=0,故x=+1,故C错误,
D.Ca是20号元素,是第四周期,第ⅡA族元素,故D错误;
故选B.
B.香花石中,Ca的电子层数大于Li、Be、O、F,Li、Be、O、F为处于同一周期的四种元素,同主族自左而右原子半径减小,非金属性增强,故原子半径Ca>Li>Be>O>F,所含金属元素中,Be的原子半径最小,故B正确;
C.该矿石中化合价分别为:Ca+2价,Be+2价,Si+4价,O-2价,F-1价,则根据化合价的原则(在化合物中正、负化合价的代数和为零),设Li元素的化合价为x,(+2)×3+x×2+[(+2)+(+4)+(-2)×4]×3+(-1)×2=0,故x=+1,故C错误,
D.Ca是20号元素,是第四周期,第ⅡA族元素,故D错误;
故选B.
点评:本题以Ca3Li2(BeSiO4)3F2为载体,考查了常见元素与常见原子团的化合价、沸点比较等知识,注意原子半径大小比较方法,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B、鸡蛋清中加入CuSO4溶液产生盐析 |
| C、乙酸乙酯、油脂与NaOH溶液反应均有乙醇生成 |
| D、石油分馏可得到汽油、煤油等 |
常温下,下列各组气体能共存(即不发生反应)的是( )
| A、NH3和HCl |
| B、NH3和SO2 |
| C、N2和O2 |
| D、NO和O2 |
氢氧燃料电池已用于航天飞机,以30%KOH溶液为电解质溶液.电极反应如下:2H2+4OH-+4e-=4H2O,O2+2H2O+4e-=4OH-. 下列说法中正确的是( )
| A、O2在负极发生还原反应 |
| B、电池总反应为2H2+O2=2H2O |
| C、该电池对环境污染很大 |
| D、燃料电池的能量转换率可达100% |
用下图所示装置进行实验,装置正确且设计合理的是( )
A、 实验室制硝基苯 |
B、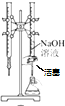 用已知浓度的NaOH溶液测定盐酸浓度的实验 |
C、 在铁制品表面镀锌操作 |
D、 称取一定量的NaOH固体 |
化学与生产、生活密切相关,下列有关说法正确的是( )
| A、生物柴油是不同酯组成的混合物,可用“地沟油”制得 |
| B、合成纤维、人造纤维及碳纤维都属于有机高分子材料 |
| C、纤维素在人体内可水解为葡萄糖,故可做人类的营养物质 |
| D、聚乙烯塑料制品可用于食品的包装,该塑料的老化是由于发生了加成反应 |
下列分子或离子中中心原子价层电子对几何构型为四面体且分子或离子空间的构型为V形的是( )
| A、NH4+ |
| B、PH3 |
| C、H3O+ |
| D、OF2 |
下列各组物质中,全部属于纯净物的一组是( )
| A、福尔马林、酒精、醋 |
| B、苯、汽油、冰醋酸 |
| C、豆油、脂肪、四氯化碳 |
| D、甘油、酒精、氯仿 |
 (14 分)CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.
(14 分)CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.