题目内容
在一定条件下,在密闭容器内将N2和H2以体积比为1∶3混合,当反应达平衡时,混合气中氨占25%(体积比),若混合前有100 mol N2,求平衡后N2、H2、NH3的物质的量及N2的转化率。
答案:
解析:
解析:
| 解:解法一:设反应消耗xmo lN2
N2+3H2ƒ2NH3 n(始)100 300 0 Dn x 3x 2x 25%= x=40 n(N2)平=(100-x)mol=(100-40)mol=60mol n(H2)平=300-3x=180mol n(NH3)平=80mol a=40/100´100%=40% 解法二:设有xmol N2反应 N2+3H2ƒ2NH3 Dn 1 2 D2 x 2x 2x 平衡时NH3的体积分数为: n(平NH3)/n(平总)´100%=n(平NH3)/(n始-Dn)=2x/(400-2x)´100%=25% ∴ x=40mol a=40%
|

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在一定条件下,在密闭容器中进行可逆反应:A(g)+B(g)?C(g)+D(g),能说明该反应达到化学平衡状态的是( )
| A、正反应和逆反应的速率相等 | B、正反应速率逐渐减小,最后为零 | C、反应停止,A、B、C、D的浓度相等 | D、A、B、C、D四种物质在密闭容器中共存 |
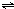 ClO(g)+3H2(g)△H>0.
ClO(g)+3H2(g)△H>0.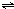 CH3OH(g)△H=-90.1kJ?mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有
CH3OH(g)△H=-90.1kJ?mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有
 C (g) + D(g),能说明该反应达到化学平衡状态的是
C (g) + D(g),能说明该反应达到化学平衡状态的是