题目内容
下列除杂过程中,所选用的试剂或方法不正确的是( )
| A、NaCl固体中有NH4Cl固体:加热 | B、自来水中含有Cl-等可溶性杂质:蒸馏 | C、Na2CO3固体中有少量NaHCO3固体:加热 | D、CO2气体中混有SO2气体:将混合气体通过盛有NaOH溶液的洗气瓶 |
分析:A.NH4Cl不稳定,加热易分解;
B.根据水易挥发的特点判断;
C.NaHCO3不稳定,加热易分解;
D.CO2和SO2都可与氢氧化钠反应.
B.根据水易挥发的特点判断;
C.NaHCO3不稳定,加热易分解;
D.CO2和SO2都可与氢氧化钠反应.
解答:解:A.NH4Cl不稳定,加热易分解生成氨气和氯化氢,可达到分离的目的,故A正确;
B.水易挥发,可用蒸馏的方法分离,故B正确;
C.NaHCO3不稳定,加热易分解,反应的方程式为2NaHCO3
Na2CO3+H2O+CO2↑,可用加热的方法除杂,故C正确;
D.CO2和SO2都可与氢氧化钠反应,应用饱和碳酸氢钠溶液除杂,故D错误.
故选D.
B.水易挥发,可用蒸馏的方法分离,故B正确;
C.NaHCO3不稳定,加热易分解,反应的方程式为2NaHCO3
| ||
D.CO2和SO2都可与氢氧化钠反应,应用饱和碳酸氢钠溶液除杂,故D错误.
故选D.
点评:本题考查物质的分离提纯,侧重于学生的分析能力、实验能力的考查,为高频考点,注意把握物质的性质异同,根据性质选择分离方法,除杂时注意不能引入新的杂质,难度不大.

练习册系列答案
相关题目
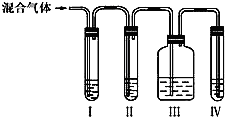 为探究乙烯与溴的加成反应:甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量浓硫酸的还原气体,由此他提出必须先除去,再与溴水反应.
为探究乙烯与溴的加成反应:甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量浓硫酸的还原气体,由此他提出必须先除去,再与溴水反应.

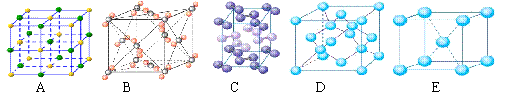
 (6)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;
(6)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;