题目内容
(1)写出下列反应的化学方程式:
①铝热反应(铝粉与四氧化三铁): ;
②铜片与过量的浓硫酸共热: ;
(2)写出下列反应的离子方程式:
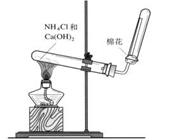
③铵盐溶液与烧碱溶液共热: ;
④铜片与浓硝酸反应: 。
(1)①8Al+3Fe3O4 4Al2O3+9Fe(条件写“点燃”也正确)
4Al2O3+9Fe(条件写“点燃”也正确)
② Cu +2H2SO4(浓) Cu SO4+SO2↑+H2O
Cu SO4+SO2↑+H2O
(2)③NH4++OH-===NH3↑+H2O ④Cu+4H++2NO3- ==Cu2++2NO2↑+2H2O
解析试题分析:铝的活泼性大于铁,可以把铁置换出来。浓硫酸具有强氧化性,因此可以与不活泼的铜反应。铵根离子与氢氧根离子反应生成氨气和水。浓硝酸具有强氧化性,因此可以与铜反应。
考点:考查常见化学反应方程式的相关知识点。

下列有关物质的性质及应用均正确的是 ( )
| A.常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B.氢氧化铁胶体具有很强的吸附性,可用于除去水中的所有杂质 |
| C.二氧化氯具有还原性,可用于自来水的杀菌消毒 |
| D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
下列有关化学反应过程的叙述中,错误的是
| A.船底镶嵌锌块,锌作负极,以防船体被腐蚀 |
| B.除去CO2中的少量SO2:通过盛有饱和NaHCO3溶液的洗气瓶 |
| C.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| D.金属钠在空气中燃烧产生黄色火焰,生成淡黄色固体 |
下列说法正确的是
| A.硅和石墨都是重要的半导体材料 |
| B.SO2、NO2、CO2都会导致酸雨的形成 |
| C.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理不同 |
| D.氢能是清洁能源,工业上用电解水法制大量氢气符合节能减排理念 |
I、铝是地壳中含量最高的金属元素,其单质及其合金在生产生活中的应用十分广泛。
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3AlF6)在熔融状态下进行电解,则化学方程式为: .其电极均由石墨材料做成,则电解时不断消耗的电极是 ;(填“阴极”或“阳极”)。
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命.以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为 ;
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,则负极的电极反应式为 ,正极附近溶液的pH (填变大、不变或变小)。
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。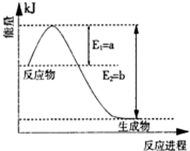
(1)图是在一定温度和压强下N2和H2反应生成1molNH3过程中能量变化示意图,请写出合成氨的热化学反应方程: (△H的数值用含字母a、b的代数式表示)。
(2)工业合成氨反应如下,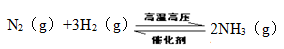
在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是 。
| A.增大压强 | B.增大反应物的浓度 | C.使用催化剂 | D.降低温度 |
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:

有3mol FeS2参加反应,转移 mol电子。
(2)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式 。
X、Y、Z、V、W是元素周期表前四周期中的五种常见元素,其相关信息如下表;
| 元素 | 相关信息 |
| X | X是形成化合物种类最多的元素,它的一种气态氧化物能产生温室效应 |
| Y | Y是地壳中含量最多的元素 |
| Z | Z和Y形成的一种化合物Z2Y2为淡黄色粉末,可作为呼吸面具里氧气的来源 |
| V | V的单质是淡黄色固体,是黑火药的一种主要成分 |
| W | W的单质是人们最早发现和使用的金属之一 |
(1)X位于第___周期____族。
(2)写出Z2Y2与水反应的离子方程式 。
(3)X和V形成的化合物是一种无色液体,其合成方法之一是一定条件下用含氢质量分数最大的有机物和V的单质为原料,同时生成一种臭鸡蛋气味的气体。请写出化学反应方程式 。
(4)已知:W2Y3(s)+3XY(g)=2W(s)+3XY2(g) △H=–26.7kJ·mol-1
3W2Y3(s)+XY(g)=2W3Y4(s)+XY2(g) △H=–50.75 kJ·mol-1
W3Y4(s)+XY(g)=3WY(s)十XY2(g) △H=–36.5 kJ·mol-1
则相同条件下,反应WY(s)+XY(g)=W(s)+XY2(g)的△H= 。

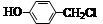 经两步反应制得,写出第一步反应的化学方程式 。
经两步反应制得,写出第一步反应的化学方程式 。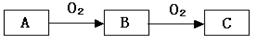
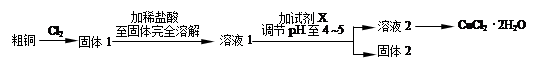

 CuCl42-(aq) +4H2O(l)
CuCl42-(aq) +4H2O(l)