题目内容
水玻璃为什么不能在空气中长期有效: .
考点:含硅矿物及材料的应用
专题:元素及其化合物
分析:水玻璃为硅酸钠的水溶液,硅酸的酸性弱于碳酸,依据强酸制弱酸的原理解答.
解答:
解:水玻璃为硅酸钠的水溶液,硅酸的酸性弱于碳酸,露置在空气中,二氧化碳与水玻璃发生反应:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓,使水玻璃变质;
故答案为:水玻璃为硅酸钠的水溶液,露置在空气中,二氧化碳与水玻璃发生反应:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓,使水玻璃变质.
故答案为:水玻璃为硅酸钠的水溶液,露置在空气中,二氧化碳与水玻璃发生反应:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓,使水玻璃变质.
点评:本题考查了硅酸钠的性质,题目难度不大,明确硅酸的酸性弱于碳酸是解题关键,注意对基础知识的积累.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
欲使醋酸溶液中的c(CH3COO-)增大且不放出气体,可向醋酸中加入少量固体( )
| A、NaOH |
| B、NaHCO3 |
| C、H2O |
| D、Mg |
下列物质中,属于电解质的是( )
| A、铜 |
| B、H2SO4 |
| C、蔗糖 |
| D、酒精 |
对于平衡体系mA(g)+nB(g)
pC(g)+qD(g)△H<0.下列结论中错误的是( )
| 催化剂 |
| △ |
| A、若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n<p+q |
| B、若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| C、若m+n=p+q,则向含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol |
| D、保持其它条件不变,升高温度,平衡向正反应方向移动 |
下列化学反应过程中,△H小于零的是( )
| A、碳跟水蒸气反应制备水煤气 |
| B、氯化铵与熟石灰共热制备氨气 |
| C、高温煅烧石灰石 |
| D、锌跟稀硫酸反应制备氢气 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、含有 NA个氦原子的氦气在标准状况下的体积约为11.2L |
| B、25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
| C、0.lmolNH4+离子中所含的电子数为1.1 NA |
| D、在标准状况下,11.2L H2O含有的分子数为0.5NA |
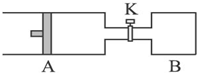 如图所示向A中充入2mol X、2mol Y,向B中充入1mol X、1mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在下,两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+2W(g);△H<0.达到平衡时,V(A)=1.2a L.
如图所示向A中充入2mol X、2mol Y,向B中充入1mol X、1mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在下,两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+2W(g);△H<0.达到平衡时,V(A)=1.2a L.