题目内容
A、B、C、D四元素的核电荷数依次增加,它们的离子的电子层数相同且最外层电子数均为8.A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半.
回答以下问题:
(1)四元素的符号依次是A________;B________;C________;D________.
它们原子半径由大到小的顺序是________.
(2)试写出四元素的离子结构简图:
A________;B________;C________;D________.它们离子的半径由大到小的顺序________.
(3)写出最高价氧化物对应水化物化学式________,分别比较酸性和碱性的强弱________.
(4)写出气态氢化物分子式_________.比较其稳定性________,理由________.
答案:略
解析:
提示:
解析:
|
(1)S ;Cl;K;Ca;r(K)>r(Ca)>r(S)>r(Cl)(2) r( 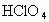 ;KOH; ;KOH;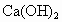 酸性: 酸性: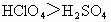 ;碱性: ;碱性: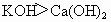 (4)HCl、 (4)HCl、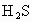 ; ;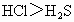 ;因氯的原子半径小于硫,氯的非金属性强 ;因氯的原子半径小于硫,氯的非金属性强 |
提示:
|
因 A原子的L层电子数与K、M层电子数之和相等,所以A的核电荷、数为2×8=16,A为硫元素.D原子的K、L层电子数之和等于电子总数的一半,所以D原子的核电荷数是(2+8)×2=20,D为钙元素.根据核电荷数依次增大,并都形成离子,排除氩原子和磷元素,B为氯元素,C为钾元素. |

练习册系列答案
相关题目
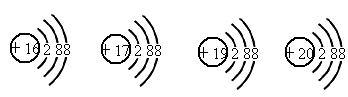
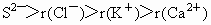 (3)
(3)