题目内容
3.下列离子方程式书写正确的是( )| A. | 用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 用小苏打治疗胃酸过多:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O | |
| D. | 偏铝酸钠溶液中通入过量CO2:AlO${\;}_{2}^{-}$+CO2+2H2O═Al(OH)3↓+HCO${\;}_{3}^{-}$ |
分析 A.电荷不守恒;
B.一水合氨为弱碱应保留化学式;
C.小苏打为碳酸氢钠,碳酸氢根离子不能拆;
D.二者反应生成氢氧化铝和碳酸氢钠.
解答 解:A.用FeCl3溶液腐蚀印刷电路板上铜箔,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故A错误;
B.AlCl3溶液中加入足量的氨水,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.用小苏打治疗胃酸过多,离子方程式:HCO3-+2H+═CO2↑+H2O,故C错误;
D.偏铝酸钠溶液中通入过量CO2,离子方程式:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意离子反应应遵循客观事实、遵循原子个数、电荷数守恒规律,题目难度不大.

练习册系列答案
相关题目
14.以下物质间的转化通过一步反应都能实现的是( )
| A. | Cl2→HClO→NaClO | B. | Fe→Fe2O3→Fe(OH)3 | ||
| C. | S→SO3→H2SO4 | D. | NH3→NO2→HNO3→NaNO3 |
18.某有机物的结构简式如图.下列关于该有机物的叙述正确的是( )


| A. | 分子中含有3种官能团 | |
| B. | 遇FeCl3溶液呈现为紫色 | |
| C. | 1mol该物质最多可与2molNaOH发生中和反应 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |
8.某饱和一元醇与浓硫酸共热得到一种无同分异构体的烯烃,该醇分子中的碳原子数一定为( )
| A. | 1 | B. | 4 | C. | 3 | D. | 6 |
15.下列金属防腐的措施中,属于牺牲阳极的阴极保护法的是( )
| A. | 水中的钢闸门连接电源的负极 | B. | 地下钢管连接锌板 | ||
| C. | 汽水底盘喷涂高分子膜 | D. | 金属护拦表面涂漆 |
12.在入住新装修的新房之前,下列做法错误的是( )
| A. | 紧闭门窗,防止装修面干裂或变质 | |
| B. | 适度开窗通风,充分进行室内外空气对流 | |
| C. | 请专业环境监测人员进行检测 | |
| D. | 在各个房间均匀地适量放置吊兰、芦荟等 |
13.辉钼(MoS2)在纳米电子设备制造领域比硅或富勒烯(如C60)更有优势.回答下列问题:
(1)钼位于第五周期VIB族.与钼相邻的上一周期同族元素的符号为Cr;该元素基态原子的电子最后排布的能级为3d,该能级上总的电子数为5.
(2)碳和硫有关数据如表:
①由上述数据可以得出,碳元素的非金属性比硫弱(填“强”或“弱”).
②写出能证明该结论的化学方程式H2SO4+Na2CO3=Na2SO4+CO2↑+H2O.
(3)从不同角度观察MoS2的晶体结构如图1,2,根据MoS2的晶体结构回答:
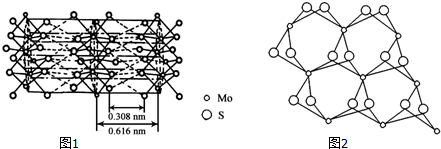
①钼的配位数为6.
②Mo与S之间的化学键为AC(填序号).
A.极性键 B.非极性键 C.配位键 D.金属键 E.范德华力
③辉钼纳米粒子的润滑性能非常优异,其原因是MoS2具有层状结构,Mo和S同层间以共价键结合,层与层之间通过范德华力结合,外力作用层与层易发生相对滑动.
(4)硅与碳在高温下反应可得到金刚砂(SiC),其结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得的金刚砂(SiC)结构.如果我们以一个硅原子为中心,设SiC晶体中硅原子与其最近的碳原子的最近距离为d,则与硅原子次近的第二层有12个原子,其离中心原子的距离是$\frac{2\sqrt{6}}{3}$d.
(1)钼位于第五周期VIB族.与钼相邻的上一周期同族元素的符号为Cr;该元素基态原子的电子最后排布的能级为3d,该能级上总的电子数为5.
(2)碳和硫有关数据如表:
| 元素 | 原子半径 | 电负性 | 第一电离能 |
| C | 67pm | 2.55 | 1125.8kJ/mol |
| S | 88pm | 2.58 | 1036.7kJ/mol |
②写出能证明该结论的化学方程式H2SO4+Na2CO3=Na2SO4+CO2↑+H2O.
(3)从不同角度观察MoS2的晶体结构如图1,2,根据MoS2的晶体结构回答:

①钼的配位数为6.
②Mo与S之间的化学键为AC(填序号).
A.极性键 B.非极性键 C.配位键 D.金属键 E.范德华力
③辉钼纳米粒子的润滑性能非常优异,其原因是MoS2具有层状结构,Mo和S同层间以共价键结合,层与层之间通过范德华力结合,外力作用层与层易发生相对滑动.
(4)硅与碳在高温下反应可得到金刚砂(SiC),其结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得的金刚砂(SiC)结构.如果我们以一个硅原子为中心,设SiC晶体中硅原子与其最近的碳原子的最近距离为d,则与硅原子次近的第二层有12个原子,其离中心原子的距离是$\frac{2\sqrt{6}}{3}$d.