题目内容
下列叙述错误的是( )
| A、用锡焊接的铁质器件,焊接处易生锈 |
| B、钢铁中含有碳,抗腐蚀能力比纯铁强 |
| C、废电池必须集中处理是为了防止电池中汞、镉和铅等重金属离子对土壤和水源造成污染 |
| D、铁管上镶嵌锌块,铁管不易被腐蚀 |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:A、金属锡和铁构成的原电池中,金属铁是负极;
B、钢铁中含有碳,金属铁和碳、电解质环境可以构成原电池,加快负极金属的腐蚀;
C、电池中汞、镉和铅等重金属离子会对土壤和水源造成污染;
D、金属锌和铁构成的原电池中,金属锌是负极,正极金属被保护.
B、钢铁中含有碳,金属铁和碳、电解质环境可以构成原电池,加快负极金属的腐蚀;
C、电池中汞、镉和铅等重金属离子会对土壤和水源造成污染;
D、金属锌和铁构成的原电池中,金属锌是负极,正极金属被保护.
解答:
解:A、所以用锡焊接的铁质器件,金属锡和铁构成的原电池中,金属铁是负极,易被腐蚀而生锈,故A正确;
B、钢铁中含有碳,金属铁和碳、电解质环境可以构成原电池,加快负极金属的腐蚀,所以钢铁中如果含有碳,抗腐蚀能力比纯铁弱,故B错误;
C、电池中汞、镉和铅等重金属离子会对土壤和水源造成污染,所以废电池必须集中处理,故C正确;
D、金属锌和铁构成的原电池中,金属锌是负极,铁是正极,正极金属铁被保护,所以铁上镶嵌锌块,铁管不易被腐蚀,故D正确.
故选B.
B、钢铁中含有碳,金属铁和碳、电解质环境可以构成原电池,加快负极金属的腐蚀,所以钢铁中如果含有碳,抗腐蚀能力比纯铁弱,故B错误;
C、电池中汞、镉和铅等重金属离子会对土壤和水源造成污染,所以废电池必须集中处理,故C正确;
D、金属锌和铁构成的原电池中,金属锌是负极,铁是正极,正极金属铁被保护,所以铁上镶嵌锌块,铁管不易被腐蚀,故D正确.
故选B.
点评:本题涉及金属的腐蚀和防护知识,注意知识的归纳和整理是关键,难度中等.

练习册系列答案
相关题目
下列化学方程式中,不能用H++OH-=H2O表示的是( )
| A、2NaOH+H2SO4=Na2SO4+2H2O |
| B、NaOH+HCl=NaCl+H2O |
| C、Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| D、KOH+HCl=KCl+H2O |
100mL 0.1mol?L-1的碳酸钠溶液所含碳酸钠的质量是( )
| A、10.6g | B、1.06g |
| C、0.53g | D、106g |
下列物质易溶于水的是( )
| A、硝酸钾 | B、氮气 |
| C、一氧化碳 | D、氯化银 |
下列烷烃在光照下与氯气反应,生成两种一氯代烃的是( )
| A、CH3CH2CH2CH2CH3 |
B、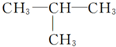 |
C、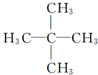 |
D、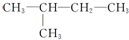 |
同属于同位素的各原子之间的关系是( )
| A、质子数相等,质量数相等 |
| B、质子数相同,中子数不同 |
| C、质子数相同,中子数相同 |
| D、质量数相同,质子数不同 |
在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是( )
| A、范德华力、范德华力、范德华力 |
| B、范德华力、范德华力、共价键 |
| C、范德华力、共价键、共价键 |
| D、共价键、共价键、共价键 |
下列收集Cl2的正确装置正确且环保的是( )
A、 |
B、 |
C、 |
D、 |
向NaBr、NaI的混合溶液中通入一定量的氯气,充分反应后将溶液蒸干并适当灼烧,最后获得的物质可能是( )
| A、NaCl、I2 |
| B、NaCl、NaBr |
| C、NaCl、NaI |
| D、NaBr、NaI |