题目内容
(10分)高铁酸钾(K2FeO4)具有很强的氧化性,是一种新型的高效水处理剂。
(1)高铁酸钾具有强氧化性的原因是 。
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为 ,___ _ _____。
(3)制备K2FeO4可以采用干式氧化法或湿式氧化法。
①干式氧化的初始反应是2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中每生成2 mol Na2FeO4时转移电子 mol。
②湿式氧化法的流程如下图:
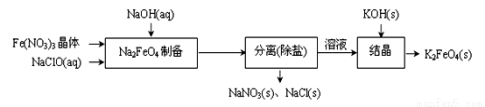
上述流程中制备Na2FeO4的化学方程式是: 。
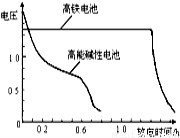
(4)高铁电池是正在研制中的可充电电池,下图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有 。
(1)其中的铁元素为+6价,易得电子(2分)
(2)高铁酸钾有强氧化性,能杀菌消毒(1分) 产生的Fe(OH)3有吸附性,有絮凝作用(1分)
(3)① 10 (2分) ② 2Fe(NO3)3 + 3NaClO +10NaOH=2Na2FeO4 +3NaCl + 6NaNO3 + 5H2O(2分)
(4)放电时间长 (1分) 工作电压稳定(1分)
【解析】
试题分析:(1)高铁酸钾中的铁是+6价,处于高价态,易得电子,具有强氧性。
(2)高铁酸钾是具有强氧性,还原产物铁离子水解生成氢氧化铁胶体,具有吸附杂质、絮凝的作用。
(3)①2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,6molNa2O2中12mol的负一价氧,2mol的有变成0价,还有10mol变成-2价,而铁是+2价变为+6价,所以每生成2mol Na2FeO4时转移电子10mol;
②Fe(NO3)3被NaClO氧化成Na2FeO4,反应的化学方程式为2Fe(NO3)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O;
(4)高铁电池由图2为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有放电时间长,工作电压稳定等优点,故答案为:放电时间长;工作电压稳定。
考点:考查高铁酸钾的性质、应用以及准备的有关判断与计算

 灵星计算小达人系列答案
灵星计算小达人系列答案下列有关化学用语表达正确的是
A.次氯酸的电子式: |
B.CCl4分子的球棍模型: |
| C.乙醛结构简式:CH3CHO |
D.H2O2的电子式: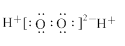 |
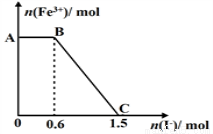
 Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,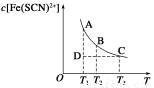
 Fe(SCN)2+(aq) ΔH>0
Fe(SCN)2+(aq) ΔH>0