题目内容
手工制陶工艺中,下列工序是在窑炉里完成的是( )
| A、烧结 | B、混合 | C、成型 | D、干燥 |
考点:陶瓷的主要化学成分、生产原料及其用途
专题:
分析:陶瓷是由石英、长石、高岭土制成的模干燥后在窑炉里烧制而成.
解答:
解:A.手工制作陶瓷一般经过:配料制备、制模、成型、干燥、施釉、装烧、装饰等,用到的原理为石英、长石、高岭土,制成的模子在窑炉里经过烧制得到陶瓷,
故选:A.
故选:A.
点评:本题考查了陶瓷的制备工艺,题目难度不大,熟悉陶瓷的烧制过程即可解答,注意相关知识的积累.

练习册系列答案
相关题目
下列实验的相关描述正确的是( )

| A、快速分离氢氧化铁胶状沉淀和氯化钠溶液可用抽滤法 |
| B、常温下,苯酚与水形成的浊液静置后会分层,上层为溶有水的苯酚溶液 |
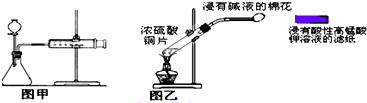
| C、甲装置可用于某些化学反应速率的测定.该装置气密性的检查如下:仪器组装好后,关闭分液漏斗活塞,将针筒活塞向外拉一段距离,然后松手,观察针筒是否能回到原来刻度处 |
| D、乙装置可用来制取和检验二氧化硫气体漂白性,待滤纸颜色褪去后立即用浸有碱液的棉花堵住试管口 |
下列关于金属钠的叙述错误的是( )
| A、金属钠可以保存在煤油中 |
| B、金属钠着火时,可用泡沫灭火器来灭火 |
| C、钠与熔融的四氯化钛反应可制取钛 |
| D、实验时用剩的钠块应该放回原试剂瓶 |
某碱性蓄电池在充电和放电时发生的反应为:Fe+NiO2+2H2O
Fe(OH)2+Ni(OH)2,下列说法中正确的是( )
| 放电 |
| 充电 |
| A、放电时,负极上发生反应的物质是Fe |
| B、放电时,正极反应是:NiO2+2e-+2H+═Ni(OH)2 |
| C、充电时,阴极反应是:Ni(OH)2-2e-+2OH-═NiO2+2H2O |
| D、充电时,阳极应该是镍元素化合价降低 |
大气污染指( )
| A、大气中含有少量的有毒、有害的物质 |
| B、大气中有毒、有害的物质可以自净到正常值 |
| C、大气中某些有毒、有害物质的含量超过正常值或大气的自净能力 |
| D、空气中氮气的含量大于氧气的含量 |
下列各组离子中,因相互促进水解,而不能大量共存的是( )
| A、Al3+、SO42-、CO32-、Cl- |
| B、Na+、HCO3-、AlO2-、Cl- |
| C、H+、HS-、Na+、SO32- |
| D、OH-、Na+、K+、HCO3- |
下列有关电解质的说法中正确的是( )
| A、物质的量相同的磷酸钠溶液和磷酸溶液中所含PO43-的量相同 | ||
B、将NaOH和氨水溶液各稀释一倍,两者OH-浓度均减少到原的
| ||
| C、强电解质溶液的导电能力不一定比弱电解质溶液强 | ||
| D、如果盐酸的浓度是醋酸浓度的二倍,则盐酸中c(H+)也是醋酸中c(H+)的二倍 |
已知2Fe2++Br2=2Fe3++2Br-.向100mL的FeBr2溶液中通入标准状况下的Cl23.36L,充分反应后测得溶液中Cl-与Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为( )
| A、2 mol/L |
| B、1 mol/L |
| C、0.4 mol/L |
| D、0.2 mol/L |