题目内容
下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
(1)③、④、⑦的原子半径由大到小的顺序为 .
(2)⑥和⑦的最高价含氧酸的酸性强弱为 > .
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为 .
(4)⑦的单质与氢氧化钠溶液反应的离子方程式为 .
(5)②与⑥最简单氢化物的稳定性强弱为 > .
(6)③与⑦氢化物的沸点高低为 > .
(7)工业上冶炼⑤的化学反应方程式为 .
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(2)⑥和⑦的最高价含氧酸的酸性强弱为
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为
(4)⑦的单质与氢氧化钠溶液反应的离子方程式为
(5)②与⑥最简单氢化物的稳定性强弱为
(6)③与⑦氢化物的沸点高低为
(7)工业上冶炼⑤的化学反应方程式为
考点:元素周期表的结构及其应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素所在周期表中的位置,可知元素的种类,①为H元素,②为O元素,③为F元素,④为Na元素,⑤为Al元素,⑥为S元素,⑦为Cl元素,
(1)电子层越多,半径越大;同周期,原子序数大的原子半径小;
(2)非金属性越强,最高价含氧酸的酸性越强;
(3)①、②两种元素的原子按1:1组成的常见液态化合物为H2O2,为共价化合物;
(4)氯气与NaOH反应生成NaCl、NaClO、水;
(5)非金属性越强,氢化物的稳定性越强;
(6)HF中含氢键,沸点高;
(7)利用电解法冶炼金属Al.
(1)电子层越多,半径越大;同周期,原子序数大的原子半径小;
(2)非金属性越强,最高价含氧酸的酸性越强;
(3)①、②两种元素的原子按1:1组成的常见液态化合物为H2O2,为共价化合物;
(4)氯气与NaOH反应生成NaCl、NaClO、水;
(5)非金属性越强,氢化物的稳定性越强;
(6)HF中含氢键,沸点高;
(7)利用电解法冶炼金属Al.
解答:
解:根据元素所在周期表中的位置,可知元素的种类,①为H元素,②为O元素,③为F元素,④为Na元素,⑤为Al元素,⑥为S元素,⑦为Cl元素,
(1)电子层越多,半径越大;同周期,原子序数大的原子半径小,则原子半径为Na>Cl>F,故答案为:Na>Cl>F;
(2)非金属性Cl>S,则最高价含氧酸的酸性为HClO4>H2SO4,故答案为:HClO4;H2SO4;
(3)①、②两种元素的原子按1:1组成的常见液态化合物为H2O2,为共价化合物,其电子式为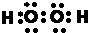 ,故答案为:
,故答案为: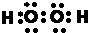 ;
;
(4)氯气与NaOH反应生成NaCl、NaClO、水,离子反应为Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(5)非金属性O>S,氢化物的稳定性为H2O>H2S,故答案为:H2O;H2S;
(6)HF中含氢键,沸点高,则沸点HF>HCl,故答案为:HF;HCl;
(7)工业上冶炼⑤的化学反应方程式为2Al2O3
4Al+3O2↑,故答案为:2Al2O3
4Al+3O2↑.
(1)电子层越多,半径越大;同周期,原子序数大的原子半径小,则原子半径为Na>Cl>F,故答案为:Na>Cl>F;
(2)非金属性Cl>S,则最高价含氧酸的酸性为HClO4>H2SO4,故答案为:HClO4;H2SO4;
(3)①、②两种元素的原子按1:1组成的常见液态化合物为H2O2,为共价化合物,其电子式为
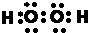 ,故答案为:
,故答案为: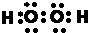 ;
;(4)氯气与NaOH反应生成NaCl、NaClO、水,离子反应为Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(5)非金属性O>S,氢化物的稳定性为H2O>H2S,故答案为:H2O;H2S;
(6)HF中含氢键,沸点高,则沸点HF>HCl,故答案为:HF;HCl;
(7)工业上冶炼⑤的化学反应方程式为2Al2O3
| ||
| ||
点评:本题考查元素周期表及元素周期律的综合应用,侧重于学生的分析能力的考查,为高考常见题型,把握元素的位置及元素的性质为解答的关键,题目难度中等.

练习册系列答案
相关题目
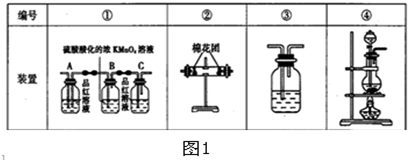
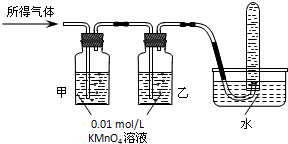
CH4中混有C2H4,欲除去C2H4得到纯净的CH4,最好依次通过盛有下列哪一组试剂的洗气瓶( )
| A、澄清石灰水,浓H2SO4 |
| B、酸性KMnO4溶液,浓H2SO4 |
| C、Br2水,浓H2SO4 |
| D、浓H2SO4,酸性KMnO4溶液 |
下列说法正确的是( )
| A、发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B、金属阳离子被还原后,不一定得到该元素的单质 |
| C、核外电子总数相同的粒子,一定是同种元素的原子 |
| D、只能与酸反应的氧化物,一定是碱性氧化物 |