题目内容
【题目】用已知物质的量浓度的酸测定未知物质的量浓度的碱时,会导致待测碱液的物质的量浓度偏低的操作是( )
①酸式滴定管在滴定前未将液面调至“0”刻度,而调在“2.40”
②碱式滴定管用蒸馏水洗后,未用待测液润洗
③滴定前酸式滴定管尖嘴部分未充满溶液,滴定后充满溶液
④滴定中不慎将锥形瓶内液体摇出瓶外
⑤滴定达终点时,视线高于滴定管内液面凹面的最低点.
A.①②④
B.②③④
C.②③⑤
D.②④⑤
【答案】D
【解析】解:①滴定时消耗的标准溶液的体积为:滴定后的读数﹣滴定前的读数,则酸式滴定管在滴定前未将液面调至“0”刻度,而调在“2.40”一样可以计算出消耗的标准溶液的体积,所以对实验无响应,则c(待测)不变;
②碱式滴定管用蒸馏水洗后,未用待测液润洗,待测液浓度偏小,待测液的物质的量偏小,滴定时消耗的标准溶液的体积偏小,根据c(待测)= ![]() 分析,可知c(待测)偏小;
分析,可知c(待测)偏小;
③滴定前酸式滴定管尖嘴部分未充满溶液,造成V(标准)偏大,根据c(待测)= ![]() 分析,可知c(待测)偏大;
分析,可知c(待测)偏大;
④滴定中不慎将锥形瓶内液体摇出瓶外,则待测溶液的物质的量减少,滴定时消耗的标准溶液的体积偏小,根据c(待测)= ![]() 分析,可知c(待测)偏小;
分析,可知c(待测)偏小;
⑤滴定达终点时,视线高于滴定管内液面凹面的最低点,读数偏小,则标准溶液的体积偏小,根据c(待测)= ![]() 分析,可知c(待测)偏小;
分析,可知c(待测)偏小;
所以会导致待测碱液的物质的量浓度偏低的操作是②④⑤;
故选D.
【考点精析】通过灵活运用酸碱中和滴定,掌握中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点即可以解答此题.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】利用催化技术可将汽车尾气中的NO和CO转变成CO2和N2 , 化学方程式如下:2NO+2CO ![]() 2CO2+N2 . 某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2+N2 . 某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/×10﹣3 molL﹣1 | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
c(CO)/×10﹣3 molL﹣1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
下列说法中,不正确的是( )
A.2s内的平均反应速率υ(N2)=1.875×10﹣4molL﹣1s﹣1
B.在该温度下,反应的平衡常数K=5
C.若将容积缩小为原来的一半,NO转化率大于90%
D.使用催化剂可以提高单位时间CO和NO的处理量
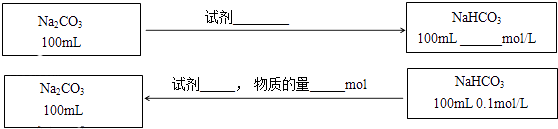
【题目】某同学在实验室研究Na2CO3和NaHCO3的性质及相互转化.
(1)分别向浓度均为0.1mol/LNa2CO3及NaHCO3溶液中滴加几滴酚酞试剂:
①Na2CO3溶液由无色变为红色,其原因是 .
②NaHCO3溶液也由无色变为红色,其原因是 .
③比较两份溶液的颜色,红色较浅的是(填化学式).
(2)研究NaHCO3与CaCl2的反应.
实验序号 | 实验操作 | 实验现象 |
实验1 | 向2mL 0.001mol/L NaHCO3溶液中加入1mL 0.1mol/LCaCl2溶液 | 无明显变化.用激光笔照射,没有出现光亮的通路. |
实验2 | 向2mL 0.1mol/L NaHCO3溶液中加入1mL 0.1mol/LCaCl2溶液 | 略显白色均匀的浑浊,用激光笔照射,出现光亮的通路. |
①实验1中没有出现白色浑浊的原因是 .
②实验2中形成的分散系属于 .
③用离子方程式表示实验2中发生的反应 .
(3)在不引入其他杂质的前提下,实现Na2CO3与NaHCO3之间的转化,请在图中标出所用的试剂、用量或物质的浓度(反应前后溶液体积的变化可忽略).