题目内容
 下列两组实验中的a、b、c都是必修教材中的常见物质,它们都有如图所示的转化关系(图中的箭头“→”表示在一定条件下,物质的转化可以一步完成),试完成下列表格.
下列两组实验中的a、b、c都是必修教材中的常见物质,它们都有如图所示的转化关系(图中的箭头“→”表示在一定条件下,物质的转化可以一步完成),试完成下列表格.
| 序号 | 已知情境 | 化学式 | 对应的离子反应方程式和现象 |
| (1) | 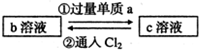 已知b溶液中滴入KSCN溶液后,溶液呈红色. |
a |
反应①的离子方程式 反应②的离子方程式 |
| (2) |  已知b为一种常见的氧化性强酸,其中某非金属元素的最高价为+5. 已知b为一种常见的氧化性强酸,其中某非金属元素的最高价为+5. |
c |
反应③的现象为 |
考点:无机物的推断
专题:推断题
分析:(1)b溶液中滴入KSCN溶液后,溶液呈红色,说明b中含有铁离子,铁离子和单质a反应生成c,c和氯气反应生成铁离子,所以c中含有亚铁离子,则a是铁;
(2)b为一种常见的氧化性强酸,且其中某非金属元素的最高价为+5,所以b是硝酸,硝酸和铜反应生成a,a能发生反应生成c气体,a能转化为c,所以a是二氧化氮,b是一氧化氮,铜和浓硝酸反应生成硝酸铜、二氧化氮和水.
(2)b为一种常见的氧化性强酸,且其中某非金属元素的最高价为+5,所以b是硝酸,硝酸和铜反应生成a,a能发生反应生成c气体,a能转化为c,所以a是二氧化氮,b是一氧化氮,铜和浓硝酸反应生成硝酸铜、二氧化氮和水.
解答:
解:(1)b溶液中滴入KSCN溶液后,溶液呈红色,说明b中含有铁离子,铁离子和单质a反应生成c,c和氯气反应生成铁离子,所以c中含有亚铁离子,则a是铁,铁和铁离子反应生成亚铁离子,亚铁离子被氯气氧化生成铁离子,则离子反应方程式分别为:2Fe3++Fe=3Fe2+、2Fe2++Cl2=2Fe3++2Cl-,
故答案为:Fe,2Fe3++Fe=3Fe2+、2Fe2++Cl2=2Fe3++2Cl-;
(2)b为一种常见的氧化性强酸,且其中某非金属元素的最高价为+5,所以b是硝酸,硝酸和铜反应生成a,a能发生反应生成c气体,a能转化为c,所以a是二氧化氮,b是一氧化氮,铜和浓硝酸反应生成硝酸铜、二氧化氮和水,铜是不溶性固体,铜盐溶液呈蓝色,二氧化氮气体呈红棕色,所以看到的现象是:固体溶解,溶液变为蓝绿色(或蓝色),产生红棕色气体,
故答案为:NO,固体溶解,溶液变为蓝绿色(或蓝色),产生红棕色气体.
故答案为:Fe,2Fe3++Fe=3Fe2+、2Fe2++Cl2=2Fe3++2Cl-;
(2)b为一种常见的氧化性强酸,且其中某非金属元素的最高价为+5,所以b是硝酸,硝酸和铜反应生成a,a能发生反应生成c气体,a能转化为c,所以a是二氧化氮,b是一氧化氮,铜和浓硝酸反应生成硝酸铜、二氧化氮和水,铜是不溶性固体,铜盐溶液呈蓝色,二氧化氮气体呈红棕色,所以看到的现象是:固体溶解,溶液变为蓝绿色(或蓝色),产生红棕色气体,
故答案为:NO,固体溶解,溶液变为蓝绿色(或蓝色),产生红棕色气体.
点评:本题考查了物质的推断,明确物质的颜色、可溶性、性质是解本题关键,注意解答时要结合a、b、c的转化图,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、氧化还原反应的本质是电子的转移 |
| B、化合反应一定是氧化还原反应 |
| C、物质中某元素失去电子,则此物质是氧化剂 |
| D、离子反应可能是复分解反应,但一定不是氧化还原反应 |
设NA代表阿伏加德罗常数的值,下列说法不正确的是( )
| A、阿伏加德罗常数NA是0.012 kg l2C中所含的原子数 |
| B、2g氢气所含氢原子数目为NA |
| C、标准状况下,11.2 L NH3所含的原子数目为0.5 NA |
| D、含71 g Na2SO4的溶液中所含Na+离子数目为NA |
①温室下取0.2mol/L的盐酸与0.2mol/LMOH等体积混合(忽略混合后溶液体积的变化),测得混合溶液的
pH=6.②室温下如果取0.2mol/LMOH溶液与0.1mol/L盐酸等体积混合,测得混合溶液的pH<7.下列说法中不正确的有( )
pH=6.②室温下如果取0.2mol/LMOH溶液与0.1mol/L盐酸等体积混合,测得混合溶液的pH<7.下列说法中不正确的有( )
| A、①中所得溶液中c(Cl-)-c(M+)=9.9×10-7mol/L |
| B、①c(H+)-c(MOH)=1×10-8mol/L |
| C、由②中信息知MOH的电离程度<M+的水解程度 |
| D、②中所得溶液中各离子浓度大小关系为:c(M+)>c(Cl-)>c(H+)>c(OH-) |
下列离子方程式书写正确的是( )
| A、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
| C、碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
| D、NaOH溶液中通入少量SO2:2OH-+SO2═SO32-+H2O |

