题目内容
下列有关说法正确的是
A.对于反应2SO2(g)+O2(g)  2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大
2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大
B.电解法精炼铜时,精铜作阳极,粗铜作阴极
C.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
D.CH3COOH溶液加水稀释后,电离程度增大,溶液中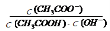 的值不变
的值不变
【答案】
D
【解析】
试题分析:A、压缩气体体积使压强增大,平衡向气体系数减小的方向移动,即向正反应方向移动,SO2的转化率增大,但平衡常数不变,错误;B、电解法精炼铜时,粗铜作阳极,精铜作阴极,错误;C、在硫酸钡悬浊液中加入足量饱和Na2CO3溶液,向所得沉淀中加入盐酸有气体产生,BaSO4沉淀转化为BaCO3沉淀,因为饱和Na2CO3溶液中CO32?浓度大,硫酸钡悬浊液中SO42?浓度很小,所以无法判断Ksp(BaSO4)与Ksp(BaCO3)的大小,错误;D、CH3COOH溶液加水稀释后,电离程度增大,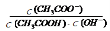 等于Ka/Kw,值不变,正确。
等于Ka/Kw,值不变,正确。
考点:本题考查化学平衡移动、电解精炼铜、沉淀溶解平衡、弱电解质电离平衡。

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
 (2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )
(2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )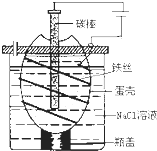 工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,
工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,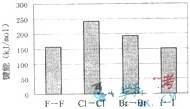 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.