题目内容
用NA表示阿伏伽德罗常数,n表示物质的量,N表示微粒数,下列不正确的是( )
| A、17gNH3所含质子数目为10NA | ||
| B、2.4g金属镁所含电子数目为0.2NA | ||
C、一个S原子的质量可表示为
| ||
| D、N=n?NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、求出氨气的物质的量n=
,而1molNH3含10mol质子;
B、求出镁的物质的量n=
,1mol镁含12mol电子;
C、1molS原子的质量为32g,而含有NA个S原子;
D、1mol任何物质中均含有NA个微粒.
| m |
| M |
B、求出镁的物质的量n=
| m |
| M |
C、1molS原子的质量为32g,而含有NA个S原子;
D、1mol任何物质中均含有NA个微粒.
解答:
解:A、氨气的物质的量n=
=
=1mol,而1molNH3含10mol质子,故A正确;
B、镁的物质的量n=
=
=0.1mol,而1mol镁含12mol电子,故0.1mol镁含1.2mol电子,故B错误;
C、1molS原子的质量为32g,而1molS含有NA个S原子,故一个S原子的质量为
g,故C正确;
D、1mol任何物质中均含有NA个微粒,故物质中的离子数N=nNA,故D正确.
故选B.
| m |
| M |
| 17g |
| 17g/mol |
B、镁的物质的量n=
| m |
| M |
| 2.4g |
| 24g/mol |
C、1molS原子的质量为32g,而1molS含有NA个S原子,故一个S原子的质量为
| 32 |
| NA |
D、1mol任何物质中均含有NA个微粒,故物质中的离子数N=nNA,故D正确.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验现象描述不正确的是( )
| A、绿豆大小的金属钠投入干燥的氯气中会激烈燃烧 |
| B、金属钠屑投入干燥的氯气中,钠屑激烈燃烧,产生黄色火星 |
| C、表面变暗的金属钠粒投入干燥氯气中,无明显现象 |
| D、在空气中点燃的金属钠伸入干燥氯气中会继续燃烧,产生光亮的黄色火焰和大量白烟 |
对Na、Mg、Al的有关性质的叙述正确的是( )
| A、碱性:NaOH<Mg(OH)2<Al(OH)3 |
| B、第一电离能:Na<Al<Mg |
| C、电负性:Na>Mg>Al |
| D、原子半径:Na<Mg<Al |
对已达到平衡的反应2X(g)+Y(g)?2Z(g)增大压强时,对反应产生的影响是( )
| A、正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
| B、正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 |
| C、正反应速率均增大,平衡向正反应方向移动 |
| D、正逆反应速率均减小,平衡向逆反应方向移动 |
已知反应2CO(g)=2C(s)+O2(g)的△H>0,△S<0,下列说法中正确的是( )
| A、低温下能自发进行 |
| B、高温下能自发进行 |
| C、任何温度下都不能自发进行 |
| D、任何温度下都能自发进行 |
下列各图所示装置属于原电池的是( )
A、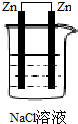 |
B、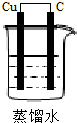 |
C、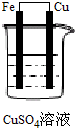 |
D、 |
如图为Fe+CuSO4=FeSO4+Cu中电子转移关系图,元素甲、乙分别表示( )


| A、Cu、Fe |
| B、Fe、Cu |
| C、Fe、O |
| D、Fe、S |
