题目内容
K2SO4的电子式 .
考点:电子式
专题:化学用语专题
分析:硫酸钾是离子化合物,由钾离子与硫酸根离子构成,钾离子的电子式为其离子符号、阴离子需要括号.
解答:
解:硫酸钾是离子化合物,由钾离子与硫酸根离子构成,硫酸钾的电子式为: ,故答案为:
,故答案为: .
.
 ,故答案为:
,故答案为: .
.
点评:本题考查电子式的书写,难度不大,要明确用电子式表示离子化合物、共价化合物、阴离子及单质分子的方法.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
近年来用合成方法制备了多种新奇的有机物,例如分子具有如图所示立体结构的环状化合物:
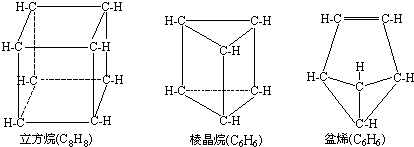
有人认为上列有机物中,①立方烷、棱晶烷可以看作是烷烃的同系物;②盆烯是单烯烃;③棱晶烷、盆烯是苯的同分异构体.上述看法正确的是( )

有人认为上列有机物中,①立方烷、棱晶烷可以看作是烷烃的同系物;②盆烯是单烯烃;③棱晶烷、盆烯是苯的同分异构体.上述看法正确的是( )
| A、①②③ | B、除①外都正确 |
| C、只有① | D、只有③ |
下列各种仪器:①漏斗、②容量瓶、③量筒、④分液漏斗、⑤天平、⑥胶头滴管、⑦蒸馏烧瓶,常用于物质分离的是( )
| A、①③⑦ | B、①④⑦ |
| C、②③⑥ | D、③④⑦ |
下列说法不正确的是( )
| A、漂白粉的有效成分是次氯酸钙 |
| B、实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钠溶液吸收 |
| C、钠、铁和铜一样都能在氯气中燃烧生成金属氯化物 |
| D、干燥的氯气可以使有色布条褪色 |
常温下,下列溶液的离子浓度关系式正确的是( )
| A、pH=4的氯化铵溶液中,c(H+)=c(NH3?H2O)=1×l0-4 mol?L-1 |
| B、pH=a的HCl溶液,稀释10倍后,其pH=b,则a=b+l |
| C、pH=2的HF溶液与pH=12的NaOH溶液体积比1:1混合:c(Na+)=c(F-)>c(H+)=c(OH-) |
| D、pH相同的①NaOH ②NaClO两种溶液中水的电离程度:①<② |
下列能用勒沙特列原理解释的是( )
| A、由二氧化硫和氧气反应制三氧化硫需要使用催化剂 |
| B、棕红色NO2加压后颜色先变深后变浅 |
| C、SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D、H2、I2、HI平衡混合气加压后颜色变深 |
下列说法中正确的是( )
| A、22.4LO2中一定含有6.02×1023个氧分子 |
| B、将80gNaOH固体溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L |
| C、18gH2O在标准状况下的体积是22.4L |
| D、在标准状况时,20mLNH3与60mLO2所含的分子数之比为1:3 |
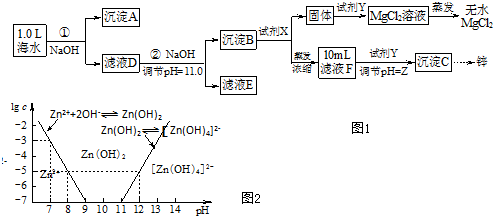
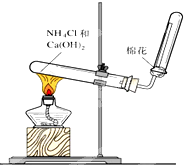 如图是实验室制取和收集氨气的装置图.回答下列问题:
如图是实验室制取和收集氨气的装置图.回答下列问题: