题目内容
4.鉴别Cl-、Br-、I-三种离子,宜选用的试剂组是( )①溴水和淀粉溶液 ②AgNO3溶液和稀硝酸 ③氯水和CCl4 ④氯水和KI-淀粉溶液.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
分析 已知还原性:I->Br->Cl-,鉴别三种离子可利用氯水分别加入到三种溶液中,能生成I2、Br2,二者颜色不同,还可加入AgNO3溶液和稀HNO3,可分别生成不同颜色的沉淀.
解答 解:①溴水不能鉴别Cl-和Br-,故错误;
②加入AgNO3溶液和稀HNO3,分别生成白色的AgCl、浅黄色的AgBr和黄色的AgI沉淀,三者颜色不同,可鉴别,故正确;
③加入氯水和CCl4溶液,能生成I2、Br2,二者颜色不同,可鉴别,故正确;
④氯水可与KI生成碘,溶液变蓝色,不能检验三种离子,用氯水和淀粉即可,故错误.
故选B.
点评 本题考查离子的鉴别,为高频考点,把握还原性的强弱、发生的反应及萃取现象为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
14.有四种混合溶液,分别由等体积0.1mol•L-1的2种溶液混合而成①CH3COONa与HCl;②CH3COONa与NaOH;③CH3COONa与NaCl;④CH3COONa与NaHCO3.下列关于该四种混合溶液的各项排序正确的是( )
| A. | pH:②>③>④>① | B. | c(CH3COO-):②>④>③>① | ||
| C. | c(H+):①>③>②>④ | D. | c(CH3COOH):①>④>③>② |
15.下列与生活有关的实验设计不合理的是( )
| A. | 用活性炭除去冰箱中的异味 | B. | 用米汤检验含碘食盐中的KIO3 | ||
| C. | 用食醋除去热水壶中的水垢 | D. | 用NaOH溶液鉴别地沟油和矿物油 |
19.19世纪末,开始揭开原子内部的秘密,最早发现电子的科学家是( )
| A. | 英国的道尔顿 | B. | 英国的卢瑟福 | C. | 丹麦的玻尔 | D. | 英国的汤姆生 |
9.下列物质:①Na ②Br2③Na2O ④NH3 ⑤CO2 ⑥蔗糖 ⑦NaCl晶体 ⑧KCl溶液 ⑨H2SO4 ⑩Ba(OH)2,其中属于电解质的是③⑦⑨⑩,属于非电解质的是④⑤⑥. (用序号填写)
16.柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是( )
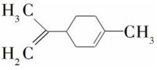

| A. | 柠檬烯的一氯代物有7种 | |
| B. | 柠檬烯和丁基苯互为同分异构体 | |
| C. | 柠檬烯的分子中所有的碳原子可能在同一个平面上 | |
| D. | 在一定条件下,柠檬烯可以发生加成、取代、氧化、还原等反应 |
13.X和Y均为短周期元素,X原子的最外层电子数是次外层电子数的2.5倍,Y原子是原子半径最小的原子,则X和Y形成的化合物的分子式可表示为( )
| A. | XY | B. | XY2 | C. | XY3 | D. | XY4 |
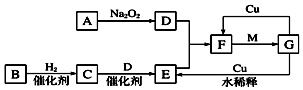
 .
.