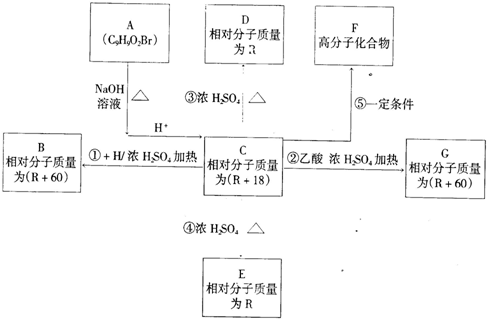
题目内容
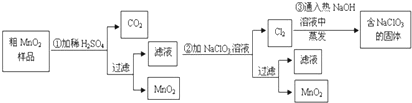
高氯酸铵可用于火箭推进剂,实验室可由NaClO3等原料制取(部分物质溶解度如图M、N),其实验流程如下:

(1)氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为 .
(2)80℃时浸取液冷却至0℃过滤,滤渣的主要成分为 (写化学式).
(3)反应器中加入氯化铵饱和溶液发生反应的离子方程式为 .
(4)已知:2NH4ClO4
N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
a.饱和食盐水 b.浓H2SO4 c.NaOH溶液 d.Mg e.Cu f.Fe
利用下图A-E装置对高氯酸铵热分解产生的三种气体进行分步吸收或收集.

①E中收集到的气体可能是 (填化学式).
②装置D的作用可能是 .
③A、B、C中盛放的药品依次可以是 (选填:Ⅰ、Ⅱ、Ⅲ).
Ⅰ.a b dⅡ.c b eⅢ.b c f.

(1)氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为
(2)80℃时浸取液冷却至0℃过滤,滤渣的主要成分为
(3)反应器中加入氯化铵饱和溶液发生反应的离子方程式为
(4)已知:2NH4ClO4
| ||
a.饱和食盐水 b.浓H2SO4 c.NaOH溶液 d.Mg e.Cu f.Fe
利用下图A-E装置对高氯酸铵热分解产生的三种气体进行分步吸收或收集.

①E中收集到的气体可能是
②装置D的作用可能是
③A、B、C中盛放的药品依次可以是
Ⅰ.a b dⅡ.c b eⅢ.b c f.
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:(1)根据题干信息:氯酸钠受热分解生成高氯酸钠和氯化钠来书写方程式;
(2)根据温度和物质的溶解度的关系知道:高氯酸钠的溶解度受温度影响大,但是氯化钠的溶解度受温度影响不大;
(3)向高氯酸钠中加入氯化铵,沉淀向着更难溶的物质转化;
(4)①根据氯气能被NaOH吸收,水可以被浓硫酸吸收,氧气可以被热的Cu吸收,氮气可以用排水法收集回答;
②根据瓶子的特点确定其用途;
③根据气体的检验顺序来回答.
(2)根据温度和物质的溶解度的关系知道:高氯酸钠的溶解度受温度影响大,但是氯化钠的溶解度受温度影响不大;
(3)向高氯酸钠中加入氯化铵,沉淀向着更难溶的物质转化;
(4)①根据氯气能被NaOH吸收,水可以被浓硫酸吸收,氧气可以被热的Cu吸收,氮气可以用排水法收集回答;
②根据瓶子的特点确定其用途;
③根据气体的检验顺序来回答.
解答:
解:据氧化还原反应原理和信息,氯酸钠受热分解生成高氯酸钠和氯化钠,可由图知,NaClO4的溶解度受温度影响很大,NaCl溶解度受温度影响不大,80℃时浸取液冷却至0℃过滤,高氯酸钠的溶解度迅速降低,析出晶体,高氯酸钠中加入氯化铵饱和溶液,反应向着更难溶的物质转化,根据物质的溶解情况,可以知道会析出高氯酸铵,过滤洗涤干燥就可以得到高氯酸铵的固体.
(1)根据氧化还原反应原理和信息,氯酸钠受热分解生成高氯酸钠和氯化钠,得到方程式为4NaClO3
3NaClO4+NaCl,故答案为:4NaClO3
3NaClO4+NaCl;
(2)可由图知,NaClO4的溶解度受温度影响很大,NaCl溶解度受温度影响不大,80℃时浸取液冷却至0℃过滤,高氯酸钠的溶解度迅速降低,析出晶体,但是氯化钠的溶解度受温度的影响不大,不会析出晶体,故答案为:NaClO4.
(3)反应器高氯酸钠中加入氯化铵饱和溶液,反应向着更难溶的物质转化,根据物质的溶解情况,可以知道会析出高氯酸铵,即发生反应的离子方
程式为NH4++ClO4-=NH4ClO4,故答案为:NH4++ClO4-=NH4ClO4;
(4)氯气能被NaOH吸收,水可以被浓硫酸吸收,氧气可以被热的Cu吸收,氮气可以用排水法收集,氢氧化钠中有水,先是吸收氯气,再是将水吸收,最后吸水的是氧气,所以A、B、C中盛放的药品依次可以是c.NaOH b.浓H2SO4 e.Cu,最后用排水法收集氮气,
①E中收集到的气体只能是氮气,故答案为:N2;
②装置D的作用以防水倒吸,所以起到安全瓶的作用,故答案为:安全瓶;
③A、B、C中盛放的药品依次可以是c.NaOH b.浓H2SO4 e.Cu,故答案为:Ⅱ.
(1)根据氧化还原反应原理和信息,氯酸钠受热分解生成高氯酸钠和氯化钠,得到方程式为4NaClO3
| ||
| ||
(2)可由图知,NaClO4的溶解度受温度影响很大,NaCl溶解度受温度影响不大,80℃时浸取液冷却至0℃过滤,高氯酸钠的溶解度迅速降低,析出晶体,但是氯化钠的溶解度受温度的影响不大,不会析出晶体,故答案为:NaClO4.
(3)反应器高氯酸钠中加入氯化铵饱和溶液,反应向着更难溶的物质转化,根据物质的溶解情况,可以知道会析出高氯酸铵,即发生反应的离子方
程式为NH4++ClO4-=NH4ClO4,故答案为:NH4++ClO4-=NH4ClO4;
(4)氯气能被NaOH吸收,水可以被浓硫酸吸收,氧气可以被热的Cu吸收,氮气可以用排水法收集,氢氧化钠中有水,先是吸收氯气,再是将水吸收,最后吸水的是氧气,所以A、B、C中盛放的药品依次可以是c.NaOH b.浓H2SO4 e.Cu,最后用排水法收集氮气,
①E中收集到的气体只能是氮气,故答案为:N2;
②装置D的作用以防水倒吸,所以起到安全瓶的作用,故答案为:安全瓶;
③A、B、C中盛放的药品依次可以是c.NaOH b.浓H2SO4 e.Cu,故答案为:Ⅱ.
点评:本题是一道物质的分离和提纯的实验方案设计题,考查学生分析和解决问题的能力,难度大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
下列化学用语中,正确的是( )
A、Mg原子结构示意图  | ||||
| B、两个硫酸根离子:SO42- | ||||
C、质子数为6、中子数为8的碳原子:
| ||||
| D、三个氧原子:3O3 |
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下: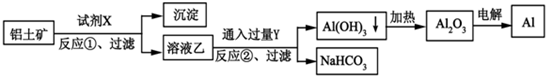
下列叙述正确的是( )

下列叙述正确的是( )
| A、试剂X可以是氢氧化钠溶液,也可以是盐酸 |
| B、反应①过滤后所得沉淀为氢氧化铁 |
| C、反应②通入的过量Y是CO2气体 |
| D、图中所示的转化反应①②都是氧化还原反应 |
生活中的一些问题常涉及到化学知识,下列叙述不正确的是( )
| A、淀粉、纤维素都是天然有机高分子化合物 |
| B、禁止使用含铅汽油是为了提高汽油的燃烧效率 |
| C、食用植物油的重要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质 |
| D、苯酚有毒,但苯酚稀溶液可用于杀菌消毒 |
自来水可用氯气消毒,某学生用自来水配制下列物质的溶液,所配溶液会变质的是( )
| A、KNO3 |
| B、FeCl2 |
| C、Na2SO4 |
| D、NaCl |