题目内容
下列实验操作正确且能达到预期目的的是
A.①⑤⑥ B.②③⑤ C.①④⑤ D.①②③④⑤⑥
| | 实验目的 | 操 作 |
| | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| | 欲证明溶液中含有SO42- | 滴入盐酸酸化的硝酸钡溶液 |
| | 欲证明溶液中含有S2- | 取少量溶液滴在醋酸铅试纸上看是否变黑 |
| | 证明SO2具有漂白性 | 将SO2通入酸性KMnO4溶液中 |
| | 比较确定铜和镁的金属活动性强弱 | 用Pt作电极电解Mg(NO3)2、Cu( NO3)2混合液 |
| | 确定碳和硅两元素非金属性强弱 | 测同温同浓度Na2CO3和Na2SiO3水溶液的PH |
A
试题分析:通过金属钠分别与水和乙醇反应,观察反应速率的快慢,可水和乙醇中羟基氢的活泼性强弱,故①正确;欲证明溶液中含有SO42-,应滴入硝酸酸化的硝酸钡溶液,因为要防止离子干扰,故②不正确;③正确,试纸变黑则证明有S2-存在;将SO2通入酸性KMnO4溶液中,溶液褪色,证明的是SO2的还原性,而不是漂白性,故④错误;⑤可通过反应的快慢来比较,正确;⑥测同温同浓度Na2CO3和Na2SiO3水溶液的PH,可确定其最高价氧化性酸相对于碱的强度,从而确定碳和硅两元素非金属性强弱,是正确的。因此,符合题意的选项为A。
点评:本题考查一些基本实验操作,学生在掌握实验操作的同时,还需要掌握其对应的实验目的,考查学生的综合分析问题的能力,难度较大。

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目

 。
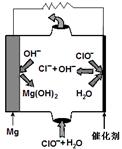
。
 CH3OH(g) +H2O(g) △H ;
CH3OH(g) +H2O(g) △H ;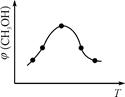
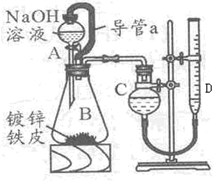


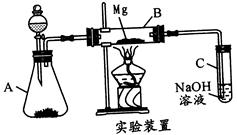
 2MgO+C的启发,用如图所示的装置进行Mg和SO2的实验。
2MgO+C的启发,用如图所示的装置进行Mg和SO2的实验。