题目内容
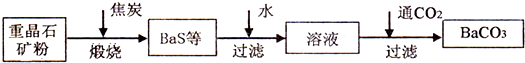
已知:BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H=+571.2kJ?mol-1
Ba(s)+S(s)+2O2(g):BaSO4(s)△H=-1473.2kJ?mol-1
Ba(s)+S(s)=BaS(g)△H=-460kJ?mol-1
请回答:
(1)C(s)和O2(g)反应生成CO(g)的热化学方程式为
(2)工业上煅烧重晶石矿粉时,为使BaSO4得到充分的还原和维持反应所需的高温,应采取的措施是
(3)沉淀转化法制备BaCO3可用饱和Na2CO3溶液将BaSO4转化为BaCO3:BaSO4(s)+CO32-(aq)=BaCO3(s)+SO42-(aq)
则:①在实验室将少量BaSO4沉淀全部转化为BaCO3的实验操作方法与步骤为
②与高温煅烧还原法相比,(用饱和Na2CO3溶液的)沉淀转化法的优点主要有
③已知:Ksp(BaCO3)=2.8×10-9,Ksp(BaSO4)=1.07×10-10.现欲用沉淀转化法将0.39mol BaSO4全部转化为BaCO3,如每次用1.00L 2.0mol?L-1Na2CO3溶液处理,至少需要处理
(2)依据平衡移动游戏因素分析;
(3)①依据碳酸钡溶度积,需要增加碳酸根离子使碳酸根离子浓度和钡离子浓度乘积大于溶度积形成碳酸钡沉淀;
②与高温煅烧还原法相比,(用饱和Na2CO3溶液的)沉淀转化法的优点是节能环保;
③依据沉淀转化结合溶度积常数计算处理将0.39mol BaSO4全部转化为BaCO3,所需操作次数;
②Ba(s)+S(s)+2O2(g)=BaSO4(s)△H=-1473.2kJ?mol-1
③Ba(s)+S(s)=BaS(g)△H=-460kJ?mol-1
依据盖斯定律②-③+①得到:4C(s)+2O2(g)=4CO(g)△H=-442kJ/mol;
得到热化学方程式为:C(s)+
| 1 |
| 2 |
故答案为:C(s)+
| 1 |
| 2 |
(2)工业上煅烧重晶石矿粉时,为使BaSO4得到充分的还原和维持反应所需的高温,平衡正向进行,应采取的措施是加入过量的炭,同时通入空气;
故答案为:加入过量的炭,同时通入空气;
(3)①在实验室将少量BaSO4沉淀全部转化为BaCO3的实验操作方法是将适量饱和Na2CO3溶液加入BaSO4沉淀中,充分搅拌,静置、弃去上层清液,如此操作,反复多次直到BaSO4全部转化为BaCO3;
故答案为:将适量饱和Na2CO3溶液加入BaSO4沉淀中,充分搅拌,静置、弃去上层清液,如此操作,反复多次(直到BaSO4全部转化为BaCO3);
②与高温煅烧还原法相比,(用饱和Na2CO3溶液的)沉淀转化法的优点主要有节约能源,无污染物生成,节能环保;
故答案为:节能,环保等;
③设每次能处理BaSO4的物质的量为x
BaSO4+CO32-═BaCO3+SO42-;
2-x x
K=
| c(SO42-) |
| c(CO32-) |
| x |
| 2.0-x |
| 1.07×10-10 |
| 2.58×10-9 |
x=0.079
外理次数
| 0.39mol |
| 0.079mol |
故答案为:5;

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
|
已知:BaSO4(s)+4C(s)=BaS(s)+4CO(g) △H=+571.2 kJ??mol-1
Ba(s)+S(s)+2O2(g):BaSO4(s) △H=—1473.2 kJ??mol-1
Ba(s)+S(s)=BaS(g) △H=—460 kJ??mol-1
请回答:
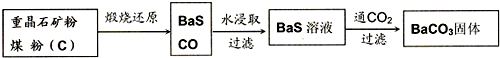
(1)工业上煅烧重晶石矿粉时,为使BaSO4得到充分还原和维持反应所需的高温,应采取的措施是 。
(2)沉淀转化法制备BaCO3可用饱和Na2CO3溶液将BaSO4转化为BaCO3:
BaSO4(s)+CO2-3(aq)=BaCO3(s)+SO2-4(aq)
则:在实验室中将少量BaSO4沉淀全部转化为BaCO3的实验操作方法与步骤为
(3)与高温煅烧还原法相比,用饱和Na2CO3溶液沉淀转化法的优点主要有
|
已知:BaSO4(s)+4C(s)=BaS(s)+4CO(g) △H=+571.2 kJ•mol-1
Ba(s)+S(s)+2O2(g):BaSO4(s) △H=—1473.2 kJ•mol-1
Ba(s)+S(s)=BaS(g) △H=—460 kJ•mol-1
请回答:
(1)工业上煅烧重晶石矿粉时,为使BaSO4得到充分还原和维持反应所需的高温,应采取的措施是 。
(2)沉淀转化法制备BaCO3可用饱和Na2CO3溶液将BaSO4转化为BaCO3:
BaSO4(s)+CO2-3(aq)=BaCO3(s)+SO2-4(aq)
则:在实验室中将少量BaSO4沉淀全部转化为BaCO3的实验操作方法与步骤为
(3)与高温煅烧还原法相比,用饱和Na2CO3溶液沉淀转化法的优点主要有
 HS-+OH-
HS-+OH-

