题目内容
10.为提纯下表所列有机物(括号内为所含的少量杂质),从(Ⅰ)中选择适宜的试剂,从(Ⅱ)中选择最佳提纯的方法,将序号填入表中.(Ⅰ)试剂:a.浓硫酸 b.氢氧化钠 c.生石灰 d.碳酸钠 e.水 f.浓溴水
(Ⅱ)方法:A.过滤 B.分液 C.蒸馏 D.蒸发
| 要提纯的物质 (少量杂质) | 溴乙烷 (乙醇) | 乙醇 (水) | 乙酸乙酯 (乙酸) | 苯 (苯酚) |
| (1)选用试剂 | ||||
| (2)分离方法 |
分析 CH3CH2Br(C2H5OH)中,加水后分层;C2H5OH(H2O)中加CaO后增大沸点差异;乙酸乙酯(乙酸)中加碳酸钠与乙酸反应;C6H6(C6H5OH)中加NaOH反应后与苯分层;
(3)分液一定需要分液漏斗.
解答 解:CH3CH2Br(C2H5OH)中,加水后分层,然后分液可除杂;C2H5OH(H2O)中加CaO后增大沸点差异,然后蒸馏可除杂;乙酸乙酯(乙酸)中加碳酸钠与乙酸反应,然后分液可除杂;C6H6(C6H5OH)中加NaOH反应后与苯分层,然后分液可除杂,故答案为:
| 要提纯的物质 (少量杂质) | 溴乙烷 (乙醇) | 乙醇 (水) | 乙酸乙酯 (乙酸) | 苯 (苯酚) |
| (1)选用试剂 | e | c | d | b |
| (2)分离方法 | B | C | B | B |
(3)分液一定需要分液漏斗,用于分层液体混合物的分离,故答案为:(梨形)分液漏斗.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握物质的性质的异同,为解答该题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
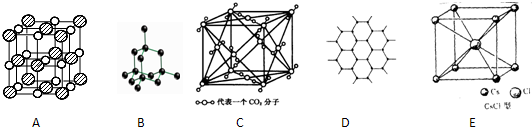
18.下列关于晶体的说法正确的是( )
| A. | 晶体中只要有阳离子就一定有阴离子 | |
| B. | 氢键属于分子间作用力,不存在于分子内 | |
| C. | 原子晶体的熔点一定比金属晶体的高 | |
| D. | 构成分子晶体的微粒不一定含有共价键 |
20.下表列出了A-F 6种元素在周期表中的位置
请回答下列问题:
(1)B、C的元素符号分别为Al、C;
(2)D、E两种元素按原子半径由小到大的顺序为O<S(用元素符号填写);
(3)F元素氢化物的化学式为HCl;
(4)A和E两元素形成的化合物的化学式为Na2S;
(5)F的单质与水反应的化学方程式为Cl2+H2O=HCl+HClO.
(6)在A~F元素中,金属性最强的元素是Na.(填元素符号)
(7)A和B的最高价氧化物对应的水化物碱性较强的是NaOH(填化学式)
(8)元素E与元素F相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是AD(可多选).
A.F的氢化物比E的氢化物稳定
B.常温下E的单质和F的单质状态不同
C.一定条件下E和F的单质都能与氢氧化钠溶液反应
D.F的最高价氧化物的水化物的酸性比E的最高价氧化物的水化物的酸性强.
| I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | |
| 2 | C | D | |||||
| 3 | A | B | E | F |
(1)B、C的元素符号分别为Al、C;
(2)D、E两种元素按原子半径由小到大的顺序为O<S(用元素符号填写);
(3)F元素氢化物的化学式为HCl;
(4)A和E两元素形成的化合物的化学式为Na2S;
(5)F的单质与水反应的化学方程式为Cl2+H2O=HCl+HClO.
(6)在A~F元素中,金属性最强的元素是Na.(填元素符号)
(7)A和B的最高价氧化物对应的水化物碱性较强的是NaOH(填化学式)
(8)元素E与元素F相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是AD(可多选).
A.F的氢化物比E的氢化物稳定
B.常温下E的单质和F的单质状态不同
C.一定条件下E和F的单质都能与氢氧化钠溶液反应
D.F的最高价氧化物的水化物的酸性比E的最高价氧化物的水化物的酸性强.
 .
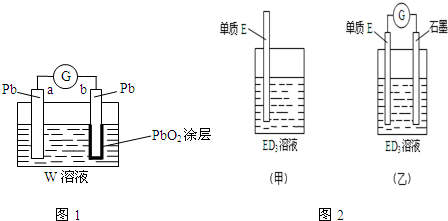
.

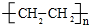 .
.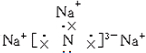 ,该化合物由离子键形成.
,该化合物由离子键形成.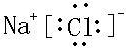 ,
, .
.