题目内容
14.下列关于元素周期表的说法不正确的是( )| A. | 除零族元素外,非金属元素全部都是主族元素 | |
| B. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| C. | 同周期ⅡA族与ⅢA族元素的原子序数之差可能为25 | |
| D. | 同族上下相邻两种元素的原子序数之差可能为32 |
分析 A、根据元素周期律判断;
B、同一周期,由左到右,得电子能力逐渐增强,非金属性增强,则第三周期非金属元素最高价含氧酸的酸性依次增强;
C、同周期第ⅡA族与第ⅢA族元素,在短周期相邻,六、七周期中相隔副族、第ⅤⅢ,且ⅢB存在锕系、镧系元素;
D、同一主族的两种元素的原子序数之差为2、8、8、18、18、32等.
解答 解:A、非金属元素(除稀有气体外)都是主族元素,故A正确;
B、同一周期,由左到右,得电子能力逐渐增强,非金属性增强,则第三周期非金属元素最高价含氧酸的酸性依次增强,非金属元素含氧酸的酸性不一定为最高价含氧酸,故B错误;
C、同周期第ⅡA族与第ⅢA族元素,若在六、七周期中相隔副族、第ⅤⅢ,且ⅢB存在锕系、镧系元素,则原子序数之差可能为25,故C正确;
D、同一主族相邻的两种元素的原子序数之差为2、8、8、18、18、32等,所以可能为32,故D正确.
故选:B.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、周期表中的族序数、原子序数等关系为解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.有一NaOH溶液长期存放在试剂瓶中,结果瓶底溶液呈浑浊状,其原因主要是( )
| A. | 吸收空气中CO2 所致 | |
| B. | NaOH与玻璃作用,而后吸收CO2 所致 | |
| C. | NaOH中含有Na2CO3 | |
| D. | 溶液中的水分部分蒸发 |
5.向盛有硫酸铜溶液的试管中滴加氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A. | 反应前后Cu2+的浓度不变 | |
| B. | 沉淀溶解后,将生成深蓝色的配离子[Cu(NH3)4]2+ | |
| C. | 向反应后的溶液中加入乙醇,溶液无明显变化 | |
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
2.将ag的铜丝灼烧变黑,趁热放入物质B中,铜丝变为红色,且质量不变,则B为( )
| A. | 盐酸 | B. | 乙醇 | C. | 醋酸 | D. | 硝酸 |
9.对反应A+3B?2C来说,下列反应速率中最快的是( )
| A. | V(B)=0.6 mol/(L•min) | B. | V(A)=0.3 mol/(L•min) | ||
| C. | V(B)=0.02/(L•S) | D. | V(C)=0.5 mol/(L•min) |
4.已知常温下,0.1mol•L-1 CH3COONH4溶液呈中性.下列有关叙述正确的是( )
| A. | 该溶液可由等体积、浓度均为0.1mol•L-1的醋酸和氨水反应得到 | |
| B. | CH3COONH4加人纯水中,水的电离程度不变 | |
| C. | 常温下,电离平衡常数K(CH3COOH)=K(NH3•H2O) | |
| D. | 该溶液中c(CH3COO-)大于同浓度CH3COONa溶液中的c(CH3COO-) |

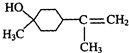 ;γ松油醇:
;γ松油醇: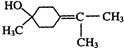 .
.