题目内容
下列物质按纯净物、混合物、电解质、非电解质的顺序组合正确的是( )
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 糖水 | 硫酸 | 铜 |
| B | 纯碱 | 石灰水 | 硫酸钡 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠溶液 | 三氧化硫 |
| D | 硝酸 | 空气 | CO2 | 乙醇 |
| A、A | B、B | C、C | D、D |
考点:电解质与非电解质,混合物和纯净物
专题:
分析:纯净物:由一种物质组成的物质;
混合物是由两种或多种物质混合而成的物质;
电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物.
混合物是由两种或多种物质混合而成的物质;
电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物.
解答:
解:A.盐酸是氯化氢的水溶液,是混合物;糖水是混合物;硫酸在水溶液中能够导电,是电解质;铜是金属单质,既不是电解质也不是非电解质,故A错误;
B.纯碱是碳酸钠,是纯净物;石灰水是氢氧化钙的水溶液,是混合物;硫酸钡在熔融状态下能够导电,是电解质;氨气自身不能电离,是非电解质,故B正确;
C.火碱是氢氧化钠,是纯净物;蔗糖溶液是混合物;氯化钠溶液是混合物,不是电解质;三氧化硫自身不能电离,是非电解质,故C错误;
D.硝酸是纯净物;空气是混合物;二氧化碳自身不能电离是非电解质;乙醇在熔融状态和水溶液中都不能导电,是非电解质,故D错误;
故选B.
B.纯碱是碳酸钠,是纯净物;石灰水是氢氧化钙的水溶液,是混合物;硫酸钡在熔融状态下能够导电,是电解质;氨气自身不能电离,是非电解质,故B正确;
C.火碱是氢氧化钠,是纯净物;蔗糖溶液是混合物;氯化钠溶液是混合物,不是电解质;三氧化硫自身不能电离,是非电解质,故C错误;
D.硝酸是纯净物;空气是混合物;二氧化碳自身不能电离是非电解质;乙醇在熔融状态和水溶液中都不能导电,是非电解质,故D错误;
故选B.
点评:本题考查纯净物、混合物、电解质、非电解质概念的辨析,难度不大.要注意基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
现有NaOH、Na2CO3、Ba(OH)2三种无色溶液,下列哪种试剂能将这三种物质鉴别( )
| A、NH4Cl |
| B、H2SO4 |
| C、AgNO3 |
| D、CuCl2 |
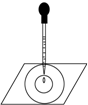 实验表明:将氯水滴加到一张蓝色石蕊试纸上,试纸上会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,下列有关说法中不正确的是( )
实验表明:将氯水滴加到一张蓝色石蕊试纸上,试纸上会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,下列有关说法中不正确的是( )| A、此实验表明氯水具有酸性、漂白性 |
| B、内环呈白色,外环呈红色或浅红 |
| C、内外环上颜色的差异表明氯水中含有H+、HClO 等粒子 |
| D、久置的氯水滴到蓝色石蕊试纸上,会出现与上述相同的现象 |
下列物质不属于电解质的是( )
| A、Cu |
| B、KOH |
| C、H2SO4 |
| D、Na2CO3 |
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
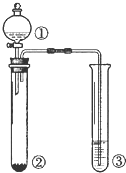

| A、①浓盐酸,②MnO2③NaOH,实验结论:制氯气并吸收尾气 |
| B、①浓硫酸,②蔗糖,③溴水,实验结论:浓硫酸具有脱水性、氧化 |
| C、①稀盐酸,②Na2SO3,③Ba(NO3)2溶液,实验结论:SO2与可溶性钡盐均可生成白色沉淀 |
| D、①浓硝酸,②Na2CO3,③Na2SiO3溶液,实验结论:酸性:硝酸>碳酸>硅酸 |
某实验室仅有如下仪器或用具:烧杯、铁架台、铁圈、三脚架、漏斗、分液漏斗、石棉网、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、火柴、滤纸.从缺少仪器角度看不能进行的实验项目是( )
| A、蒸发 | B、萃取 | C、过滤 | D、蒸馏 |
关于下列图示的说法中正确的是( )
A、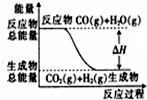 表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”中的△H>0 |
B、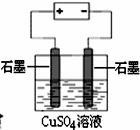 为电解硫酸铜溶液的装置,电解前后溶液的pH几乎不变 |
C、 实验装置可完成比较乙酸、碳酸、硅酸酸性强弱的实验 |
D、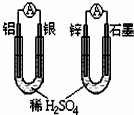 两个装置通过的电量相等时,消耗负极材料的物质的量也相同 |