题目内容
10.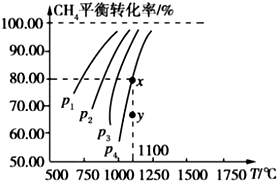 在一恒容的密闭容器中充入 0.1mol/L CO2、0.1mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )
在一恒容的密闭容器中充入 0.1mol/L CO2、0.1mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )| A. | 1100℃时该反应平衡常数为 1.64 | B. | 压强:p4>p3>p2>p1 | ||
| C. | 上述反应的△H<0 | D. | 压强为 p4时,在y点:v 正>v 逆 |
分析 A、反应 CH4(g)+CO2(g)?2CO(g)+2H2(g),
起始(mol/L) 0.1 0.1 0 0
变化(mol/L) 0.08 0.08 0.16 0.16
平衡(mol/L) 0.02 0.02 0.16 0.16
平衡常数K=$\frac{0.1{6}^{2}×0.1{6}^{2}}{0.02×0.02}$=1.64,由此解答.
B、增大压强,平衡向气体体积减小的方向移动;
C、利用三段式计算出平衡时的浓度求算;随温度的升高转化率增大;
D、y点时甲烷的转化率小,平衡正向移动.
解答 解:A、反应 CH4(g)+CO2(g)?2CO(g)+2H2(g),
起始(mol/L) 0.1 0.1 0 0
变化(mol/L) 0.08 0.08 0.16 0.16
平衡(mol/L) 0.02 0.02 0.16 0.16
平衡常数K=$\frac{0.1{6}^{2}×0.1{6}^{2}}{0.02×0.02}$=1.64,故A正确;
B、压强增大,平衡向逆反应方向移动,甲烷的转化率变小,故P4>P3>P2>P1,故B正确;
C、从图象分析,随温度升高转化率增大,正反应吸热,△H>0,故C错误;
D、在y点,甲烷的转化率小于平衡时的转化率,平衡正向移动,V正>V逆,故D正确.
故选C.
点评 本题考查了平衡受温度、压强的影响而移动的问题,注意看准图象是解题的关键,难度中等.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案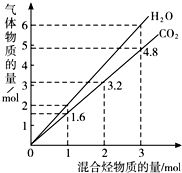 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )①一定有乙烯 ②一定有甲烷 ③一定有丙烷
④一定没有乙烷 ⑤可能有甲烷 ⑥可能有乙炔.
| A. | ②⑤⑥ | B. | ②⑥ | C. | ②④ | D. | ②③ |
| A. | 葡萄糖和果糖 | B. | 氧气和臭氧 | C. | 正丁烷和正戊烷 | D. | 金刚石和石墨 |
| A. |  和 和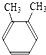 | B. | CH3CH2OH和CH3 CH2-O-CH2CH3 | ||
| C. | 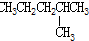 和 和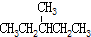 | D. | 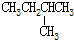 和 和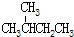 |
| A. | CH3CH2CH3 和 CH3CH(CH3)CH3 | B. |  和 和  | ||
| C. | CH3COOCH2CH3和CH3COOH | D. | CH3CH2CHO和CH3CH2CH2OH |
| A. | 2个甲基,能生成4种一氯代物 | B. | 3个甲基,能生成3种一氯代物 | ||
| C. | 3个甲基,能生成5种一氯代物 | D. | 4个甲基,能生成5种一氯代物 |
| A. | C3H5Cl的链状同分异构体有6种(考虑顺反异构) | |
| B. |  能发生氧化反应、取代反应、加成反应和消去反应 能发生氧化反应、取代反应、加成反应和消去反应 | |
| C. | 分子式符合C4H8O2的酸类和酯类同分异构体共有4种 | |
| D. | 丙烯分子内所有原子都在同一个平面 |
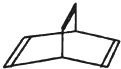 有机物的结构可用“键线式”简化表示,如:CH3一CH=CH-CH3可表示为
有机物的结构可用“键线式”简化表示,如:CH3一CH=CH-CH3可表示为 ,有一种有机物X的键线式如图所示.
,有一种有机物X的键线式如图所示. ;
;