题目内容
下列有关说法正确的是A.物质熔沸点的高低顺序是:晶体硅>氯化钠>冰>氖气
B.粒子半径由大到小顺序是:H->Li+>H+
C.溶液中结合H+能力由强到弱的顺序是:![]() >H2PO
>H2PO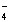 >CH3COO->
>CH3COO->![]()
D.CO2、HClO、CF4、PCl3四种物质分子中的所有原子都满足最外层为8电子的稳定结构
AB
解析:晶体硅是原子晶体,熔沸点最高,氯化钠是离子晶体,熔沸点较高,冰和氖气形成的分子晶体熔沸点较低,常温下水是液态,氖是气态,故冰的熔沸点大于氖气,A正确;H-和Li+核外电子排布相同,H-的核电荷数比Li+小,所以H-半径大于Li+半径,H+核外没有电子,故半径最小,B正确;因为H2SO4、H3PO4、CH3COOH、H2CO3的酸性减弱,所以结合H+的能力是![]() <
<![]() <CH3COO-<
<CH3COO-<![]() ,C不正确;HClO中H原子不满足最外层为8电子的稳定结构,D不正确。
,C不正确;HClO中H原子不满足最外层为8电子的稳定结构,D不正确。

练习册系列答案
相关题目
 (2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )
(2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )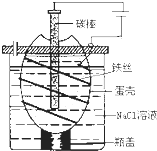 工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,
工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,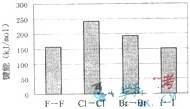 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.