题目内容
同温同压下,比较等质量的CO气体和CO2气体的叙述中正确的是( )
| A、密度比为7:11 |
| B、体积比为7:11 |
| C、原子个数比为11:7 |
| D、分子个数比为11:7 |
考点:物质的量的相关计算
专题:计算题
分析:同温同压下,气体摩尔体积相等,根据ρ=
、V=
Vm、n=
、N=
NA结合分子构成分析解答.
| M |
| Vm |
| m |
| M |
| m |
| M |
| m |
| M |
解答:
解:同温同压下,气体摩尔体积相等,CO、CO2的摩尔质量分别是28g/mol、44g/mol,
A.根据ρ=
知,气体密度与其摩尔质量成正比,所以其密度之比等于其摩尔质量之比=28g/mol:44g/mol=7:11,故A正确;
B.根据V=
Vm知,相同质量、相同气体摩尔体积时,其体积之比等于其摩尔质量的反比=44g/mol:28g/mol=11:7,故B错误;
C.根据N=
NA知,相同质量时,其分子数之比等于其摩尔质量的反比=44g/mol:28g/mol=11:7,每个CO、CO2分子中原子个数之比为2:3,所以总的原子个数之比22:21,故C错误;
D.根据N=
NA知,相同质量时,其分子数之比等于其摩尔质量的反比=44g/mol:28g/mol=11:7,故D正确;
故选AD.
A.根据ρ=
| M |
| Vm |
B.根据V=
| m |
| M |
C.根据N=
| m |
| M |
D.根据N=
| m |
| M |
故选AD.
点评:本题考查了物质的量的有关计算,熟悉物质的量的有关公式是解本题关键,再结合基本公式中各个物理量之间的关系式解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某种解热阵痛药的结构简式如图,关于该物质的说法正确的是( )


| A、分子中含有一个肽键,是一种二肽 |
| B、当它完全水解时,可得到的产物有4种 |
| C、该物质苯环上的一硝基取代物有6种 |
D、水解产物之一为 ,该物质显酸性的异构体有3种(包括其本身) ,该物质显酸性的异构体有3种(包括其本身) |
下列叙述正确的是( )
| A、氯化钠溶液能导电,所以氯化钠溶液是电解质 |
| B、化合反应不一定是氧化还原反应 |
| C、盐、碱一定含有金属元素 |
| D、在水溶液中电离产生H+的化合物一定是酸 |
下列离子反应方程式正确的是( )
| A、碳酸氢钠溶液跟过量的饱和石灰水反应 HCO3-+Ca2++OH-=CaCO3↓+2H2O |
| B、向NaHSO4溶液中滴加Ba(OH)2溶液显中性H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| C、氯化亚铁溶液中通入氯气 Fe2++Cl2=Fe3++2Cl- |
| D、苛性钾溶液中加入稀醋酸 H++OH-=H2O |
下列叙述错误的是( )
| A、用金属钠可区分乙醇和乙醚 |
| B、用高锰酸钾酸性溶液可区分苯和甲苯 |
| C、用水可区分苯和溴苯 |
| D、用新制的银氨溶液可区分甲酸甲酯和乙醛 |
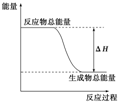 下列物质间的反应,其能量变化符合图的是( )
下列物质间的反应,其能量变化符合图的是( )| A、由氢气与氧气反应 |
| B、灼热的炭与二氧化碳反应 |
| C、Ba(OH)2?8H2O晶体和NH4Cl晶体混合 |
| D、碳酸钙的分解 |
常温下,下列各溶液的叙述中不正确的是( )
| A、c(NH4+)相同的NH4Cl溶液和(NH4)2SO4溶液,二者的pH相等 |
| B、pH=7的醋酸钠和醋酸混合液中:c(Na+)=c(CH3COO-) |
| C、0.1 mol?L-1的醋酸的pH=a,0.01 mol?L-1的醋酸的pH=b,则a+1>b |
| D、已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,[c(Na+)-c(F-)]<[c(K+)-c(CH3COO-)] |
下列说法中,不正确的是( )
| A、金属单质和盐溶液的反应都属于置换反应 |
| B、质量数相等的不同核素,一定属于不同种元素 |
| C、Al2O3既能与强碱反应,又能与强酸反应,所以Al2O3属于两性氧化物 |
| D、等物质的量的C2H6和H2O2含电子数相同 |
下列关于卤族元素的递变规律不正确的是( )
| A、F2、Cl2、Br2、I2的氧化性逐渐减弱 |
| B、HF、HCl、HBr、HI的热稳定性逐渐减弱 |
| C、F-、Cl-、Br-、I-的还原性逐渐增强 |
| D、F2、Cl2、Br2、I2的密度逐渐增大,熔沸点逐渐减小 |