题目内容
20.N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)?4NO2(g)+O2(g)△H>0;一定温度下,向10L恒容密闭容器中通入N2O5,的部分实验数据见下表:| t/s | 0 | 500 | 1000 | 1500 |
| n(N2O5)/mol | 5.00 | 3.5 | 2.50 | 2.50 |
| A. | 500s内N2O5分解速率为3×10-4mol•L-1•s-1 | |
| B. | 反应达平衡后,往容器中加入5molN2O5气体,平衡正向移动,反应的热效应不变 | |
| C. | 相同温度下,将体积缩小为原来的$\frac{1}{2}$,达到新平衡时,N2O5(g)的浓度为0.125mol/L | |
| D. | 达到新平衡的压强是初始时的1.75倍 |
分析 A.500s内N2O5的浓度变化量为(5-3.5)mol=1.5mol,根据v=$\frac{△c}{△t}$计算v(N2O5);
B.增大反应物浓度,平衡正向移动,化学计量数不变,反应热不变;
C.相同温度下,将体积缩小为原来的$\frac{1}{2}$,若平衡不移动,同种组分的浓度变为原来的2倍,等效为增大压强,平衡逆向移动,平衡移动不能消除浓度增大,则达到新平衡时,N2O5(g)的浓度小于0.5mol/L,大于0.25mol/L
D.由表中数据可知,T1温度下,1000s时反应到达平衡,平衡时n(N2O5)=2.5mol,则:
2N2O5(g)?4NO2(g)+O2(g)
起始量(mol):5 0 0
变化量(mol):2.5 5 1.25
平衡量(mol):2.5 5 1.25
恒温恒容下,压强之比等于混合气体总物质的量之比.
解答 解:A.500s内N2O5的浓度变化量为(5-3.5)mol=1.5mol,则v(N2O5)=$\frac{\frac{1.5mol}{10L}}{500s}$=3×10-4 mol/(L•s),故A正确;
B.往容器中加入5molN2O5气体,N2O5浓度增大,平衡正向移动,热化学方程式中化学计量数不变,反应热不变,故B正确;
C.相同温度下,将体积缩小为原来的$\frac{1}{2}$,若平衡不移动,同种组分的浓度变为原来的2倍,等效为增大压强,平衡逆向移动,平衡移动不能消除浓度增大,则达到新平衡时,N2O5(g)的浓度小于0.5mol/L,大于0.25mol/L,故C错误;
D.由表中数据可知,T1温度下,1000s时反应到达平衡,平衡时n(N2O5)=2.5mol,则:
2N2O5(g)?4NO2(g)+O2(g)
起始量(mol):5 0 0
变化量(mol):2.5 5 1.25
平衡量(mol):2.5 5 1.25
恒温恒容下,压强之比等于混合气体总物质的量之比,达到新平衡的压强是初始时的$\frac{8.75mol}{5mol}$=1.75倍,故D正确,
故选:C.
点评 本题考查化学平衡有关计算、化学平衡影响因素等,难度中等,注意理解掌握外界条件对平衡移动的影响.

| A. | 将CO2通入BaCl2溶液中至饱和,无沉淀产生,再通入SO2,产生白色沉淀 | |
| B. | 已知CuS和FeS都难溶于水,将H2S分别通入CuCl2和FeCl2溶液,都会产生沉淀 | |
| C. | 向AlCl3溶液中滴加NaHCO3溶液,产生白色沉淀;再加入NaHSO4溶液,沉淀可消失 | |
| D. | 形状基本一样的纯净锌块和含铜、铁等杂质的锌块分别与相同浓度的稀硫酸反应纯净的锌块反应产生氢气的速率快 |
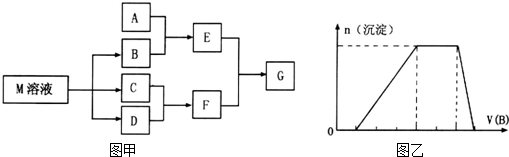

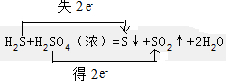 .
.