题目内容
在1L的密闭容器中,充入1mo1CO和1mo1H2O (g),于850℃时进行化学反应:CO(g)+H2O (g) CO2(g)+H2(g)△H<0,达平衡时,有50%的CO转化为CO2.在相同温度下,将1mo1CO和4mo1H2O (g)充入同样的容器中,记录0~8分钟内测得容器内各物质的物质的量如下表.下列说法正确的是( )
CO2(g)+H2(g)△H<0,达平衡时,有50%的CO转化为CO2.在相同温度下,将1mo1CO和4mo1H2O (g)充入同样的容器中,记录0~8分钟内测得容器内各物质的物质的量如下表.下列说法正确的是( )| 时间/min | n(CO)/mo1 | n(H2O)/mo1 | n(CO2)/mo1 | n(H2)/mo1 |
| 1 | 4 | |||
| 4 | 0.25 | 3.25 | 0.75 | 0.75 |
| 6 | n1 | n2 | n3 | n4 |
| 8 | n1 | n2 | n3 | n4 |
A.前4min,用CO表示的化学反应速率为v(CO)=0.25mol/
B.反应在第4 min时处于化学平衡状态
C.8分钟时,混合气体中CO2的体积分数为16%
D.若初始条件相同,绝热下进行上述反应,6 min时n(CO)>n1
【答案】分析:CO(g)+H2O (g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始(mol/L):1 1 0 0
转化(mol/L):0.5 0.5 0.5 0.5
平衡(mol/L):0.5 0.5 0.5 0.5
k=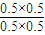 =1,
=1,
在相同温度下,将1mo1CO和4mo1H2O (g)充入同样的容器中,设平衡时转化了xmolCO,
CO(g)+H2O (g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始(mol/L):1 4 0 0
4min时:0.25 3.25 0.75 0.75
平衡转化(mol/L):x x x x
平衡(mol/L):1-x 4-x x x
则4min时浓度商Q=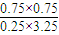 =0.69<1,说明还没有达到平衡状态,
=0.69<1,说明还没有达到平衡状态,
平衡时: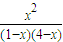 =1,x=0.8,
=1,x=0.8,
以此解答该题.
解答:解:A.前4min,用CO表示的化学反应速率为v(CO)=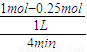 =0.1875/(L?min),故A错误;
=0.1875/(L?min),故A错误;
B.CO(g)+H2O (g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始(mol/L):1 1 0 0
转化(mol/L):0.5 0.5 0.5 0.5
平衡(mol/L):0.5 0.5 0.5 0.5
k=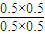 =1,
=1,
在相同温度下,将1mo1CO和4mo1H2O (g)充入同样的容器中,设平衡时转化了xmolCO,
CO(g)+H2O (g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始(mol/L):1 4 0 0
4min时:0.25 3.25 0.75 0.75
平衡转化(mol/L):x x x x
平衡(mol/L):1-x 4-x x x
则4min时浓度商Q=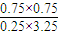 =0.69<1,说明还没有达到平衡状态,故B错误;
=0.69<1,说明还没有达到平衡状态,故B错误;
C.由表中数据可知6min和8min时各物质的物质的量不变,说明达到平衡状态,由B计算可知平衡时: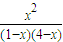 =1,
=1,
x=0.8,反应前后气体的体积不变,则8分钟时,混合气体中CO2的体积分数为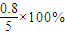 =16%,故C正确;
=16%,故C正确;
D.若初始条件相同,绝热下进行上述反应,因反应放热,则体系温度逐渐升高,由于反应放热,升高温度平衡向逆反应方向移动,则6 min时n(CO)>n1,故D正确.
故选CD.
点评:本题考查化学平衡的计算,题目难度中等,注意利用三段式法计算较为直观,计算平衡常数为解答该题的关键.
 CO2(g)+H2(g)
CO2(g)+H2(g)起始(mol/L):1 1 0 0
转化(mol/L):0.5 0.5 0.5 0.5
平衡(mol/L):0.5 0.5 0.5 0.5
k=
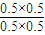 =1,
=1,在相同温度下,将1mo1CO和4mo1H2O (g)充入同样的容器中,设平衡时转化了xmolCO,
CO(g)+H2O (g)
 CO2(g)+H2(g)
CO2(g)+H2(g)起始(mol/L):1 4 0 0
4min时:0.25 3.25 0.75 0.75
平衡转化(mol/L):x x x x
平衡(mol/L):1-x 4-x x x
则4min时浓度商Q=
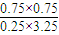 =0.69<1,说明还没有达到平衡状态,
=0.69<1,说明还没有达到平衡状态,平衡时:
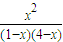 =1,x=0.8,
=1,x=0.8,以此解答该题.
解答:解:A.前4min,用CO表示的化学反应速率为v(CO)=
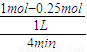 =0.1875/(L?min),故A错误;
=0.1875/(L?min),故A错误;B.CO(g)+H2O (g)
 CO2(g)+H2(g)
CO2(g)+H2(g)起始(mol/L):1 1 0 0
转化(mol/L):0.5 0.5 0.5 0.5
平衡(mol/L):0.5 0.5 0.5 0.5
k=
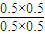 =1,
=1,在相同温度下,将1mo1CO和4mo1H2O (g)充入同样的容器中,设平衡时转化了xmolCO,
CO(g)+H2O (g)
 CO2(g)+H2(g)
CO2(g)+H2(g)起始(mol/L):1 4 0 0
4min时:0.25 3.25 0.75 0.75
平衡转化(mol/L):x x x x
平衡(mol/L):1-x 4-x x x
则4min时浓度商Q=
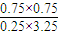 =0.69<1,说明还没有达到平衡状态,故B错误;
=0.69<1,说明还没有达到平衡状态,故B错误;C.由表中数据可知6min和8min时各物质的物质的量不变,说明达到平衡状态,由B计算可知平衡时:
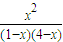 =1,
=1,x=0.8,反应前后气体的体积不变,则8分钟时,混合气体中CO2的体积分数为
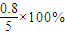 =16%,故C正确;
=16%,故C正确;D.若初始条件相同,绝热下进行上述反应,因反应放热,则体系温度逐渐升高,由于反应放热,升高温度平衡向逆反应方向移动,则6 min时n(CO)>n1,故D正确.
故选CD.
点评:本题考查化学平衡的计算,题目难度中等,注意利用三段式法计算较为直观,计算平衡常数为解答该题的关键.

练习册系列答案
相关题目
(2011?宣城二模)T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H=-49.0kJ?mol-1测得H2和CH3OH(g)的浓度随时间变化如下图所示.下列说法不正确的是( )
|
在1L的密闭容器中,充入1mol CO和1mol H2O (g),于850℃时进行化学反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,达平衡时,有50%的CO转化为CO2.在相同温度下,将1mol CO和4mol H2O(g)充入同样的容器中,记录0~8分钟内测得容器内各物质的物质的量如下表.t分钟时为改变条件后达平衡时所测得的数据.下列说法正确的是( )
| 时间/min | n(CO)/mol | n(H2O)/mol | n(CO2)/mol | n(H2)/mol |
| 0 | 1 | 4 | 0 | 0 |
| 4 | 0.25 | 3.25 | 0.75 | 0.75 |
| 6 | n1 | n2 | n3 | n4 |
| 8 | n1 | n2 | n3 | n4 |
| t | 0.15 | 3.15 | 0.85 | 0.85 |
| A、前4min,用CO表示的化学反应速率为v(CO)=0.25mol/(L?min) |
| B、反应在第4min时处于化学平衡状态 |
| C、8分钟时,混合气体中CO2的体积分数为16% |
| D、t分钟时,反应所处的温度高于850℃ |
 (2010?朝阳区模拟)T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.0kJ/mol测得H2和CH3OH(g)的浓度随时间变化如图所示.下列说法不正确的是( )
(2010?朝阳区模拟)T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.0kJ/mol测得H2和CH3OH(g)的浓度随时间变化如图所示.下列说法不正确的是( )