题目内容
 如图为一种原电池装置图,电解质溶液为稀硫酸,回答下列问题:
如图为一种原电池装置图,电解质溶液为稀硫酸,回答下列问题:(1)此时灯泡
(2)Mg电极上发生的反应为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)该装置符合原电池构成条件,所以能构成原电池,放电时有电流产生;
(2)镁易失电子发生氧化反应作负极、Al作正极,正极上氢离子得电子发生还原反应.
(2)镁易失电子发生氧化反应作负极、Al作正极,正极上氢离子得电子发生还原反应.
解答:
解:(1)该装置符合原电池构成条件,所以能构成原电池,放电时有电流产生,则小灯泡亮,故答案为:亮;
(2)镁易失电子发生氧化反应作负极、Al作正极,正极上氢离子得电子发生还原反应,负极电极反应为 Mg-2e-=Mg2+、正极电极反应为2H++2e-=H2↑,故答案为:Mg-2e-=Mg2+.
(2)镁易失电子发生氧化反应作负极、Al作正极,正极上氢离子得电子发生还原反应,负极电极反应为 Mg-2e-=Mg2+、正极电极反应为2H++2e-=H2↑,故答案为:Mg-2e-=Mg2+.
点评:本题考查了原电池原理,明确正负极的判断方法是解本题关键,再结合电极上发生的反应即可解答,注意电解质溶液酸碱性影响正负极的判断,为易错点.

练习册系列答案
相关题目
第一个绘制出化学元素周期表的科学家是( )
| A、门捷列夫 | B、阿伏伽德罗 |
| C、戴维 | D、道尔顿 |
依据元素周期表及元素周期律,下列推断正确的是( )
| A、H3BO3的酸性比H2CO3的强 |
| B、氢氧化钡的碱性比氢氧化钙的碱性强 |
| C、硒化氢比硫化氢稳定 |
| D、若Xm+ 和Yn- 核外电子层结构相同,则在周期表中X、Y的族序数之差一定为:(m+n)-8 |
向明矾[KAl(SO4)2?12H2O]溶液中加入Ba(OH)2溶液,当SO42-恰好沉淀完全时,这时铝元素的存在形式是( )
| A、Al(OH)3沉淀 |
| B、只有〔AlO2〕-离子 |
| C、Al(OH)3沉淀和Al3+ |
| D、Al(OH)3沉淀和〔AlO2〕-离子 |
 在2L密闭容器中,800℃时反应2NO(g)+O2(g)→2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)→2NO2(g)体系中,n(NO)随时间的变化如表: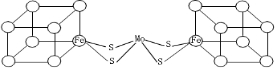 .图中左右两边对称,各含一个近似立方体的结构.每个立方体含有4个Fe原子和4个S原子,它们位于立方体的8个顶点,且原子间只有一种化学键.
.图中左右两边对称,各含一个近似立方体的结构.每个立方体含有4个Fe原子和4个S原子,它们位于立方体的8个顶点,且原子间只有一种化学键.