题目内容
8.“部分酸、碱和盐的溶解性表(室温)”是学习化学的重要工具,下表是截取溶解性表中的一部分,有关①处物质的说法不正确的是( )| 阴离子 阳离子 | OH- | Cl- |
| … | … | … |
| Fe2+ | 不 | ① |
| … | … | … |
| A. | ①处物质的化学式是FeCl2 | B. | ①处物质的名称是氯化铁 | ||
| C. | ①处物质可溶于水 | D. | ①处物质类别属于盐 |
分析 依据图中内容可知①物质阳离子为亚铁离子,阴离子为氯离子,所以为氯化亚铁,氯化亚铁可溶于水,是由金属阳离子与酸根离子构成,据此分析解答.
解答 解:依据图中内容可知①物质阳离子为亚铁离子,阴离子为氯离子,所以为氯化亚铁,氯化亚铁可溶于水,是由金属阳离子与酸根离子构成,符合盐的概念属于盐,所以ACD正确,
故选:B.
点评 本题考查了物质的分类和性质,明确酸、碱、盐、氧化物概念,熟悉氯化亚铁性质是解题关键,题目难度不大.

练习册系列答案
相关题目
18. 国庆期间对大量盆栽鲜花施用了S诱抗素制剂,以保证鲜花盛开.S诱抗素的分子结构如图.下列关于该物质的说法正确的是( )
国庆期间对大量盆栽鲜花施用了S诱抗素制剂,以保证鲜花盛开.S诱抗素的分子结构如图.下列关于该物质的说法正确的是( )
 国庆期间对大量盆栽鲜花施用了S诱抗素制剂,以保证鲜花盛开.S诱抗素的分子结构如图.下列关于该物质的说法正确的是( )
国庆期间对大量盆栽鲜花施用了S诱抗素制剂,以保证鲜花盛开.S诱抗素的分子结构如图.下列关于该物质的说法正确的是( )| A. | 该有机物的分子式为C15H22O4 | |
| B. | 该有机物能发生取代、加成和酯化反应 | |
| C. | 1 mol该有机物与足量溴反应最多消耗4 mol Br2 | |
| D. | 1 mol该有机物与足量Na反应生成2 mol H2 |
19.把2g氢氧化钠固体分别加入下列100ml的溶液中,溶液的导电性基本不变的是( )
| A. | 自来水 | B. | 0.5mol/L盐酸 | ||
| C. | 0.5mol/L醋酸 | D. | 0.5mol/L氢氧化钠溶液 |
16.下列叙述不正确的是( )
| A. | 易溶于水的物质一定是电解质 | |
| B. | 有化学键断裂的变化不一定是化学变化 | |
| C. | 溶解于水所得溶液能导电的物质不一定是电解质 | |
| D. | 水受热不易分解,与水分子之间存在的氢键无关 |
13.已知甲与乙反应生成丙和丁,某实验小组对这一反应进行定量测定,测定结果如表所示.下列有关说法正确的是( )
| 甲 | 乙 | 丙 | 丁 | 反应状况 | |
| 实验一 | 32g | 40g | mg | 9g | 甲与乙恰好完全反应 |
| 实验二 | 16g | 30g | 0.25mol | amol |
| A. | 甲的摩尔质量为32g•mol-1 | |
| B. | 实验二中甲与乙也恰好完全反应 | |
| C. | 若丁的摩尔质量为18g•mol-1,则a=0.5 | |
| D. | 丙的摩尔质量为126g•mol-1 |
20.目前,已经合成了LiH、NaH、CaH2、MgH2(AlH3)n等,下列说法不正确的是( )
| A. | 金属氢化物都是强还原剂 | |
| B. | 金属与H2制备金属氢化合物时,H2作还原剂 | |
| C. | 金属氢化物与水反应生成对应的碱和H2 | |
| D. | 离子半径:r(H-)>r(Li+) |
16.现有两种烯烃:CH2=CH2和 它们的混合物进行聚合反应,则聚合反应的产物中含有如下四种物质中的( )
它们的混合物进行聚合反应,则聚合反应的产物中含有如下四种物质中的( )

 它们的混合物进行聚合反应,则聚合反应的产物中含有如下四种物质中的( )
它们的混合物进行聚合反应,则聚合反应的产物中含有如下四种物质中的( )
| A. | ①③④ | B. | ③ | C. | ②③ | D. | ①②④ |
17.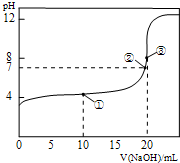 25℃时,用 0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LCH3COOH溶液所得滴定曲线如图.下列叙述正确的是( )
25℃时,用 0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LCH3COOH溶液所得滴定曲线如图.下列叙述正确的是( )
 25℃时,用 0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LCH3COOH溶液所得滴定曲线如图.下列叙述正确的是( )
25℃时,用 0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LCH3COOH溶液所得滴定曲线如图.下列叙述正确的是( )| A. | 点①所示溶液:c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| B. | 点②所示溶液:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | |
| C. | 点③所示溶液:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定终点时:c(CH3COOH)+c(CH3COO-)=c(Na+ ) |