题目内容
2.根据下列实验操作和现象所得结论不正确的是( )| 选项 | 实验操作和现象 | 结论 |
| A | 用玻璃棒蘸取某溶液进行焰色反应实验,火焰呈黄色 | 溶液中含有Na+ |
| B | 向浓度均为0.1mol•L-1的FeCl3和AlCl3混合溶液中滴加NaOH溶液,出现红褐色沉淀. | Ksp[Fe(OH)3]<Ksp[Al(OH)3] |
| C | 室温下,用pH试纸测得:0.1mol•L-1 Na2CO3溶液的pH约为11;0.1mol•L-1 NaHCO3溶液的pH约为8. | HCO3-结合H+的能力比CO32-的强 |
| D | 用Fe3+浓度相同的FeCl3溶液和Fe2(SO4)3溶液,分别清洗做完银镜反应的试管,FeCl3溶液清洗得干净 | 存在可逆过程:Fe3++Ag?Fe2++Ag+,且溶解度AgCl<Ag2SO4 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.焰色反应为元素的性质,钠的焰色反应为黄色;
B.Ksp小的先沉淀;
C.盐中酸根离子对应酸越弱,水解程度越大;
D.氯化银的溶解度比硫酸银的溶解度小.
解答 解:A.焰色反应为元素的性质,钠的焰色反应为黄色,则由现象可知溶液中含有Na+,故A正确;
B.Ksp小的先沉淀,由现象可知Ksp[Fe(OH)3]<Ksp[Al(OH)3],故B正确;
C.盐中酸根离子对应酸越弱,水解程度越大,由现象可知,Na2CO3溶液水解程度大,则HCO3-酸性小于碳酸的酸性,即HCO3-结合H+的能力比CO32-的弱,故C错误;
D.氯化银的溶解度比硫酸银的小,Fe3++Ag?Fe2++Ag+,FeCl3溶液中的氯离子能使平衡向右移动,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握焰色反应、沉淀转化、平衡移动为解答本题的关键,侧重分析与实验能力的考查,注意化学反应原理及实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
12. 利用如图所示装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测其中现象正确的是( )
利用如图所示装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测其中现象正确的是( )
 利用如图所示装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测其中现象正确的是( )
利用如图所示装置进行实验,将仪器a中的溶液滴入b中,根据c中所盛溶液,预测其中现象正确的是( )| 选项 | a | b | c | c试管中现象 |
| A | 浓盐酸 | KMnO4 | FeCl2溶液 | 溶液变棕黄色 |
| B | 稀硫酸 | Na2S2O3 | 溴水 | 产生浅黄色沉淀 |
| C | 硼酸 | Na2CO3 | Na2SiO3溶液 | 析出白色沉淀 |
| D | 浓硝酸 | 铁片 | KI-淀粉溶液 | 溶液变蓝色 |
| A. | A | B. | B | C. | C | D. | D |
10.如图表示AlCl3溶液与NaOH溶液相互滴加过程中微粒的关系曲线,下列判断正确的是( )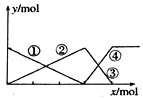

| A. | ①线表示AlO2-的物质的量的变化 | B. | x表示AlCl3的物质的量 | ||
| C. | ③线表示Al(OH)3的物质的量的变化 | D. | ④线表示AlO2-的物质的量的变化 |
17.下列反应的离子方程式书写正确的是( )
| A. | 金属钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | NaHCO3的水解反应:HCO3-+H2O?CO32-+H3O+ | |
| C. | 铁和稀HNO3反应后溶液pH=1:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | 向Mg(HCO3)2溶液中加入过量NaOH溶液:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O |
7.物质的量浓度相同的CsCl、SrCl2、CrCl3三种溶液,当溶液的体积比为3:2:1时,三种溶液中Cl-的物质的量浓度之比为( )
| A. | 6:3:2 | B. | 1:2:3 | C. | 3:2:1 | D. | 1:1:1 |
4.在酸性溶液中,Fe2O42-易转化为Fe2+,其反应过程为Fe2O42-+H+-Fe2++H2O.现有KMnO4、Na2CO3、Cu2O、HNO3四种物质,其中一种物质能使上述反应发生,下列说法正确的是( )
| A. | 能使上述反应发生的物质是KMnO4 | |
| B. | 该氧化还原反应的离子方程式中水的计量数为5 | |
| C. | 该氧化还原反应中氧化剂是Fe2O42-,发生氧化反应 | |
| D. | 有1mol还原剂参与反应时,转移4NA个电子 |
5.氯化铵晶体溶于重水中,生成物的化学式为( )
| A. | NH2D•H2O | B. | NH3•DHO | C. | HD2O+ | D. | NH3•D2O |

