题目内容
6.常温下,一种烷烃A和一种单烯烃B组成的混合气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多.(1)将1L混合气体充分燃烧,在同温同压下得到2.5LCO2气体.试通过计算推断原混合气体中A和B所有可能的组合及其体积比,并将结果填入下表:
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比(VA:VB) |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
(2)120℃时,取1L该混合气体与9L氧气混合,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大了6.25%.试通过计算确定唯一符合题意的A、B的分子式C2H6、C4H8.
分析 (1)根据1L碳原子数为n的烷烃或烯烃充分燃烧后均得到n升CO2,由题意(1L混合气体充分燃烧后生成2.5升CO2,且B分子的碳原子数比A分子的多)可推断,混合气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成,它们有四种可能的组合,根据每一种组合中烷烃和烯烃的碳原子数及燃烧后生成的CO2体积,利用十字交叉法可确定A和B的体积比;
(2)根据燃烧方程式利用差量法来计算.
解答 解:(1)因1升混合气体充分燃烧后生成2.5升CO2,且B分子的碳原子数比A分子的多,混合气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成.它们有四种可能的组合:CH4、C3H6;CH4、C4H8;
C2H6、C3H6;C2H6、C4H8;根据每一种组合中烷烃和烯烃的碳原子数及燃烧后生成的CO2体积,可确定A和B的体积比.如: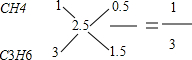 ,即V(CH4):V(C3H6)=1:3,
,即V(CH4):V(C3H6)=1:3,
所以①CH4、C3H6、1:3;②CH4、C4H8、1:1③C2H6、C3H6、1:1④C2H6、C4H8、3:1;
故答案为:
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比(VA:VB) |
| ① | CH4 | C3H6 | 1:3 |
| ② | CH4 | C4H8 | 1:1 |
| ③ | C2H6 | C3H6 | 1:1 |
| ④ | C2H6 | C4H8 | 3:1 |
(2)设1L气态烃与氧充分燃烧后体积变化为△V升,则
CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O(气)△V1=0(升)
C2H6+O2$\stackrel{点燃}{→}$2CO2+3H2O(气)△V2=0.5(升)
C3H6+$\frac{9}{2}$O2$\stackrel{点燃}{→}$3CO2+3H2O(气)△V3=0.5(升)
C4H8+6O2$\stackrel{点燃}{→}$4CO2+4H2O(气)△V4=1.0(升)
各种组合的1升混合气体与氧气充分燃烧,体积增大为
组合①$\frac{△V1+3△V3}{4}$=0.375(升)
组合②$\frac{△V1+△V4}{2}$=0.5(升)
组合③$\frac{△V2+△V3}{2}$=0.5(升)
组合④$\frac{3△V2+△V4}{4}$=0.625(升) 则$\frac{0.625}{10}$×100%=6.25%,
故组合④符合题意,即A:C2H6;B:C4H8.
故答案为:C2H6、C4H8.
点评 本题主要考查了十字交叉法、差量法的使用,有一定的难度,注意根据燃烧的方程式进行判断,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
17.下列叙述中正确的是( )
| A. | Ba(OH)2的电离方程式为:Ba(OH)2?Ba2++(OH)22- | |
| B. | 易溶于水的物质一定是电解质,难溶于水的物质一定不是电解质 | |
| C. | 硫酸铝熔化时发生了电离,可表示为:Al2(SO4)═2Al3++3SO42- | |
| D. | 虽然CO2水溶液的导电能力较弱,但CO2仍是电解质 |
1.在2L密闭容器中,把2mol X和2mol Y混合,发生如下反应:3X(g)+Y(g)═nP(g)+2Q(g),当反应经2min达到平衡,测得P的浓度为0.8mol/L,Q的浓度为0.4mol/L,则下列判断中,不正确的是( )
| A. | n=4 | |
| B. | X的转化率为60% | |
| C. | X的平衡浓度为0.4mol/L | |
| D. | 2 min内Y的平均速率为0.4mol/(L.min) |
15.在两个容积相同的容器中,一个盛有O2气体,另一个盛有CO2和HCl的混合气体.在同温同压下,两容器内的气体一定具有相同的是( )
| A. | 原子数 | B. | 密度 | C. | 质量 | D. | 分子数 |
16.下列设计的实验方案能达到实验目的是( )
| A. | 制备Al(OH)3悬浊液:向1mol•L-1AlCl3溶液中加过量的6mol•L-1NaOH溶液 | |
| B. | 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和氢氧化钠溶液,振荡后静置分液,并除去有机相的水 | |
| C. | 检验溶液中是否含有Fe2+:取少量待检验溶液,向其中滴加KSCN溶液,再加入少量新制氯水,观察实验现象 | |
| D. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
