题目内容
15.实验室需要0.2mol/L CuSO4溶液240mL,实验室可提供配制溶液的试剂有:①蓝色胆矾晶体(CuSO4•5H2O) ②4mol/L CuSO4溶液(1)无论采用何种试剂进行配制,实验必须用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,至少还需要的一种仪器是250mL容量瓶.
(2)若用胆矾晶体进行配制,需用托盘天平称取CuSO4•5H2O的质量为12.5g;如果用4mol/L
的CuSO4溶液稀释配制,需用量筒量取12.5ml 4mol/L CuSO4溶液.
(3)实验室用4mol/L的硫酸铜溶液稀释配制溶液所需的实验步骤有:
①往烧杯中加入约100ml水进行初步稀释,冷却至室温
②用量筒量取一定体积4mol/L 的硫酸铜溶液于一烧杯中
③计算所需4mol/L 硫酸铜溶液的体积
④将溶液颠倒摇匀后转存于试剂瓶
⑤加水至液面离容量瓶1-2cm处改用胶头滴管进行定容
⑥洗涤烧杯和玻璃棒2-3次并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
⑦将溶液转移入容量瓶
其中正确的操作顺序为:③②①⑦⑥⑧⑤④
(4)配制溶液过程中,如果出现以下情况,对结果有何影响(填“偏高”、“偏低”或“无影响”)
A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线偏低
B.定容时俯视刻度线偏高
C.容量瓶未干燥即用来配制溶液无影响
D.量筒用蒸馏水洗后未干燥就用来量取4mol/L的CuSO4溶液偏低
E.将烧杯中的溶液转移到容量瓶时,未用水洗涤烧杯偏低.
分析 (1)依据配制一定物质的量浓度溶液步骤选择需要仪器;
(2)依据m=CVM计算需要溶质的质量;依据稀释前后溶质的物质的量不变计算需要硫酸铜的体积,依据硫酸铜体积选择量筒规格;
(3)依据配制一定物质的量浓度溶液步骤排序;
(4)分析不当操作对溶质的物质的量和溶液的体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)配制一定物质的量浓度溶液步骤有:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,用到的仪器有:托盘天平、药匙、烧杯、玻璃棒
250mL容量瓶、胶头滴管,
故答案为:250mL容量瓶;
(2)配制0.2mol/L CuSO4溶液240mL,应选择250mL容量瓶,实际配制250mL溶液,需要CuSO4•5H2O的质量m=0.2mol/L×0.25L×250g/mol=12.5g;
如果用5mol/L的CuSO4溶液稀释配制,设需要浓硫酸铜溶液的体积为V,依据稀释前后溶质的物质的量不变,4mol/L×V=0.2mol/L×250mL,12.5mL;
解得V=12.5mL;
故答案为:12.5;12.5;
(3)用浓溶液配制一定物质的量浓度溶液步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,所以正确的顺序为:③②①⑦⑥⑧⑤④;
故答案为:③②①⑦⑥⑧⑤④;
(4)A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,导致溶液的体积偏大,溶液的浓度偏低;
故答案为:偏低;
B.定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏高;
故答案为:偏高;
C.容量瓶未干燥即用来配制溶液,对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变;
故答案为:无影响;
D.量筒用蒸馏水洗后未干燥就用来量取4mol/L的CuSO4溶液,导致浓硫酸铜溶液被稀释,量取的溶液中含有硫酸铜的物质的量偏小,溶液浓度偏低;
故答案为:偏低;
E.将烧杯中的溶液转移到容量瓶时,未用水洗涤烧杯,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,
故答案为:偏低;
点评 本题考查了配制一定物质的量浓度的溶液的方法,明确配制原理是解题关键,注意量筒、容量瓶规格的选择依据,注意误差分析的方法和技巧.

| A. | 碳 | B. | 氧 | C. | 硅 | D. | 硫 |
| A. | 14g由N2和13C2H2组成的混合物所含的电子数为7NA | |
| B. | 标准状况下,11.2L NO与11.2L O2混合后所含的分子数小于0.75NA | |
| C. | 常温下,1L PH=3的Al2(SO4)3溶液中,水电离出的H+数目为10-3NA | |
| D. | 在100mL 1 mol•L-5 Na2S02溶液与1.12 L(标准状况)CL2的反应中,•还原剂失电子0.2NA |

已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图2所示:
Ⅱ.有关物质的溶度积如下
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
(2)热的Na2CO3溶液有较强的去油污能力,其原因是(用离子方程式及必要的文字加以解释)Na2CO3在溶液中存在水解平衡CO32-+H2O?HCO3-+OH-,溶液呈碱性,当温度升高时水解平衡正向移动,使溶液碱性增强,故去油污能力增强.
(3)“趁热过滤”时的温度应控制在高于36℃.
(4)已知:Na2CO3•10H2O(s)═Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)═Na2CO3•H2O(s)+9H2O(g)△H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式Na2CO3•H2O(S)═Na2CO3(s)+H2O(g)△H=+58.73kJ/mol.
(5)有人从“绿色化学”角度设想将“母液”沿流程图中虚线所示进行循环使用.请你分析实际生产中是否可行不可行,其理由是若“母液”循环使用,则溶液c(Cl-)和c(SO42-)增大,最后所得产物Na2CO3中混有杂质.
| A. | 向某溶液中加入稀盐酸产生无色无味的可使澄清石灰水变浑浊的气体,则原溶液中一定含有CO32- | |
| B. | 向某溶液中加入氯化钡溶液有白色沉淀产生,再加入稀盐酸,沉淀不消失,则原溶液中一定含有SO42- | |
| C. | 向某溶液中加入碳酸钠溶液产生白色沉淀,再加入盐酸,白色沉淀消失,则原溶液中一定含有Ba2+ | |
| D. | 向某溶液中加入硝酸酸化的硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl- |
| A. | 六氟化氙(XeF6) | B. | 次氯酸(HClO) | C. | 氯化硫(S2Cl2) | D. | 白磷(P4) |
| A. | PAFC用于净化饮用水时,比用相同量的氯化铝或氯化铁对水的pH改变大 | |
| B. | PAFC中铁为+2价 | |
| C. | PAFC可看作一定比例的氯化铝和氯化铁的水解产物 | |
| D. | PAFC在强酸性或强碱性溶液中都能稳定存在 |
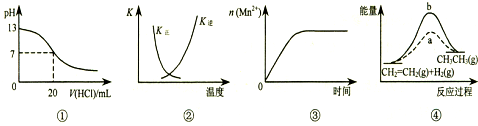
| A. | 图①表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 | |
| C. | 图③表示10 mL 0.01 mol•L-1 KMnO4 酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | 图④中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
| A. | 裂化可以提高汽油等轻质油的产量和质量 | |
| B. | 硬脂酸甘油酯皂化反应后得到的主要产品是硬脂酸和甘油 | |
| C. | 乙醇、乙酸、乙酸乙酯分子中均存在-OH | |
| D. | 向2 mL苯中加入1 mL碘的CCl4溶液,振荡后静置,上层呈紫红色 |