题目内容
7.下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素.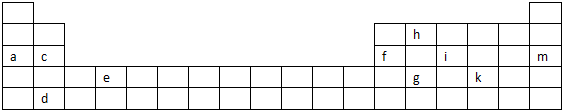
(1)表中所列元素中,属于短周期元素的有Na、Mg、Al、C、P、Ar(写元素符号),e元素在元素周期表中的位置是四周期,ⅣB族.
(2)下列D组元素的单质可能都是电的良导体.
A、a,c,h B、i,g,k C、c,h,m D、d,e,f
(3)i元素属于非金属(填金属或非金属)元素,它的最高正化合价是+5、负化合价是-3.它能跟氧气反应,生成一种吸水性很强的物质,这种物质在实验室里常用做干燥剂,写出它跟氧气反应的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
分析 由元素周期表中元素的位置,可以a是Na,c是Mg,d是Sr,e是Ti,f是Al,g是Ge,h是C,i是P,k是Se,m是Ar.
(1)第一、二、三周期为短周期;由位置可知e处于第四周期ⅣB族;
(2)金属元素单质是电的良导体;
(3)i是P,属于非金属元素;最高正化合价=族序数=最外层电子数、最大负化合价=最外层电子数-8;它能跟氧气反应,生成一种吸水性很强的物质,这种物质在实验室里常用做干燥剂,则该氧化物为P2O5.
解答 解:由元素周期表中元素的位置,可以a是Na,c是Mg,d是Sr,e是Ti,f是Al,g是Ge,h是C,i是P,k是Se,m是Ar.
(1)第一、二、三周期为短周期,故上述元素中Na、Mg、Al、C、P、Ar处于短周期;由位置可知e处于第四周期ⅣB族,故答案为:Na、Mg、Al、C、P、Ar;四、ⅣB;
(2)金属元素单质是电的良导体,选项中只有D中全部为金属元素,故选:D;
(3)i是P,属于非金属元素;最外层电子数为5,故高正化合价为+5、最大负化合价=5-8=-3;它能跟氧气反应,生成一种吸水性很强的物质,这种物质在实验室里常用做干燥剂,则该氧化物为P2O5,反应方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,故答案为:非金属;+5;-3;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
点评 本题考查元素周期表及其应用,需要学生熟练注意元素周期表,有利于基础知识的巩固.

练习册系列答案
相关题目
17.下列现象与氢键的作用有关的是( )
①NH3、HF、H2O的熔、沸点比同族其他元素氢化物的高
②乙醇、乙酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④尿素[CO(NH2)2]的熔、沸点比醋酸的高
⑤DNA的结构和生物活性
⑥水分子高温下也很稳定
⑦SiO2的硬度大,熔沸点高
⑧干冰用于人工降雨
⑨SO3与水的反应是放热反应.
①NH3、HF、H2O的熔、沸点比同族其他元素氢化物的高
②乙醇、乙酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④尿素[CO(NH2)2]的熔、沸点比醋酸的高
⑤DNA的结构和生物活性
⑥水分子高温下也很稳定
⑦SiO2的硬度大,熔沸点高
⑧干冰用于人工降雨
⑨SO3与水的反应是放热反应.
| A. | ①②③④⑤ | B. | ②③④⑤⑥⑦ | C. | ①②④⑤⑨ | D. | ①②③⑤⑧ |
18.“化学,我们的生活,我们的未来”曾经是2011年“国际化学年”的主题.你认为下列行为中,不符合这一主题的是( )
| A. | 控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源 | |
| B. | 大量使用化肥和农药,以提高农作物产量 | |
| C. | 开发太阳能、水能、风能等新能源、减少使用煤、石油等化石燃料 | |
| D. | 实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle) |
15.下列说法不正确的是( )
| A. | 无论乙烯与丙烯酸以何种比例混合,只要二者总物质的量是个定值,完全燃烧时所消耗的氧气也一定是个定值 | |
| B. | 鉴别甲苯、苯乙烯、苯酚、丙烯酸溶液可选用KMnO4溶液、溴水 | |
| C. | 苯中的少量苯酚可先加适量的浓溴水,使苯酚生成三溴苯酚,再过滤而除去 | |
| D. | 苯酚的酸性很弱,但可以和Na2CO3反应 |
19.下列有关反应速率的说法正确的是( )
| A. | 用铁片和稀硫酸反应制氢气时,改用98%的硫酸可以加快反应速率 | |
| B. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | SO2的催化氧化反应是一个放热的反应,所以升高温度,反应速率变慢 | |
| D. | 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率变慢 |
16.MCFC型燃料电池可同时供应电和水蒸气,其工作温度为600℃~700℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2=2H2O,则下列有关该电池的说法正确的是( )
| A. | 随着反应的进行,CO32-在不断消耗 | |
| B. | 该电池的正极的反应式为:4OH-+4e-=O2+2H2O | |
| C. | 放电时CO32-向正极移动 | |
| D. | 该电池负极的反应为:H2+CO32--2e-=H2O+CO2 |
17.23Na与23Na+比较,相同的是( )
| A. | 微粒半径 | B. | 化学性质 | C. | 最外层电子数 | D. | 中子数 |
 已知:
已知: .
.