题目内容
16.我国的“神舟五号’,载人飞船己发射成功,“嫦娥”探月工程也己正式启动.据科学家预测,月球的土壤中吸附着数百万吨的${\;}_{2}^{3}$He,每百吨${\;}_{2}^{3}$He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以${\;}_{2}^{4}$He的形式存在.下列说法正确的是( )| A. | ${\;}_{2}^{4}$He原子核内含有4个质子 | B. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | ||
| C. | ${\;}_{2}^{3}$He原子核内含有3 个中子 | D. | ${\;}_{2}^{4}$He具有较强的金属性 |
分析 A.根据原子符号ZAX的含义,A表示质量数,Z表示质子数,中子数=质量数-质子数;
B.质子数相同,中子数不同的原子互称为同位素;
C.中子数=质量数-质子数;
D.He原子最外层2个电子是稳定结构.
解答 解:A.24He原子核内含有2个质子,故A错误;
B.23He和24He质子数相同,中子数不同,故互为同位素,故B正确;
C.23He的质子数为2,质量数为3,中子数为3-2=1,故C错误;
D.因He原子的结构稳定,既不容易得到电子,也不容易失去电子,故D错误.
故选B.
点评 本题主要考查了原子符号的含义、核素的种类以及同位素的概念,难度不大,明确概念是解答本题关键.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
7.下列叙述正确的是( )
| A. | CH2ClCH2Cl的系统命名是二氯乙烷 | |
| B. | 四氯化碳的电子式是 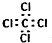 | |
| C. | 乙烯的最简式是C2H4 | |
| D. | 2,5-二甲基己烷的核磁氢谱中出现三组峰 |
11.要将溴水中的溴提取出来,需要用到的一组仪器是( )
| A. | 普通漏斗、玻璃棒、烧杯 | B. | 长颈漏斗、玻璃棒、烧杯 | ||
| C. | 大试管、试管夹、容量瓶 | D. | 分液漏斗、烧杯、铁架台 |
1.下列描述,其因果关系成立的是( )
| A. | 因为NH3的水溶液可以导电,所以NH3是电解质 | |
| B. | 因为O2可以与CO反应生成CO2,所以可以用O2除去CO2中的杂质CO | |
| C. | 因为液态HCl不导电,所以HCl是非电解质 | |
| D. | 因为氢氧化铁胶体具有吸附性,所以常用于净水 |
8.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A. | 离子半径大小顺序:r(Z2+)>r(Y2-) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应水化物的酸性比W的弱 | |
| D. | Y的气态简单氢化物的热稳定性比W的强 |
6.下列离子方程式书写正确的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++ClO-+Cl- | |
| B. | 向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O?Al(OH)3(胶体)+3H+ | |
| C. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| D. | 氯化铁溶液可用制作印刷电路板:Cu+Fe3+═Cu2++Fe2+ |