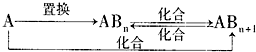题目内容
下列叙述正确的是
- A.Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
- B.Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2
- C.Na2O具有氧化性,Na2O2具有还原性
- D.Na2O2具有漂白性
D
碱性氧化物是指能与酸反应生成盐和水的氧化物,这里所说的反应仅限于复分解反应,不包括氧化还原反应:
Na2O+2HCl=2NaCl+H2O
2Na2O2+4HCl=4NaCl+2H2O2
 2H2O+O2↑
2H2O+O2↑
可见,Na2O是碱性氧化物,而Na2O2不是。A选项错。
置换反应是指单质和化合物相互结合生成另外的单质和化合物的反应。
2Na2O2+2CO2══2Na2CO3+O2
没有单质参加反应,不是置换反应。B选项错。
氧化性是得电子能力,还原性是失电子能力。一般说来,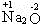 不能再得电子,没有氧化性;
不能再得电子,没有氧化性;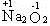 中O元素为-1价,还能得电子,应具有氧化性,由Na2O2与H2O的反应,又知其也有还原性:
中O元素为-1价,还能得电子,应具有氧化性,由Na2O2与H2O的反应,又知其也有还原性:
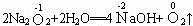 Na2O2是强氧化剂,具有漂白性,D选项对。
Na2O2是强氧化剂,具有漂白性,D选项对。
碱性氧化物是指能与酸反应生成盐和水的氧化物,这里所说的反应仅限于复分解反应,不包括氧化还原反应:
Na2O+2HCl=2NaCl+H2O
2Na2O2+4HCl=4NaCl+2H2O2
 2H2O+O2↑
2H2O+O2↑可见,Na2O是碱性氧化物,而Na2O2不是。A选项错。
置换反应是指单质和化合物相互结合生成另外的单质和化合物的反应。
2Na2O2+2CO2══2Na2CO3+O2
没有单质参加反应,不是置换反应。B选项错。
氧化性是得电子能力,还原性是失电子能力。一般说来,
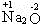 不能再得电子,没有氧化性;
不能再得电子,没有氧化性;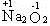 中O元素为-1价,还能得电子,应具有氧化性,由Na2O2与H2O的反应,又知其也有还原性:
中O元素为-1价,还能得电子,应具有氧化性,由Na2O2与H2O的反应,又知其也有还原性: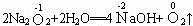 Na2O2是强氧化剂,具有漂白性,D选项对。
Na2O2是强氧化剂,具有漂白性,D选项对。 
练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
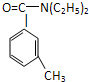 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH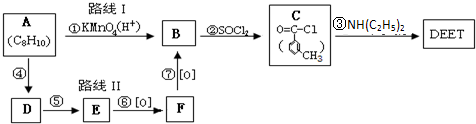
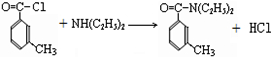
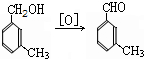
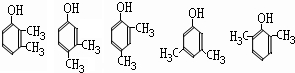 (任写2种)
(任写2种)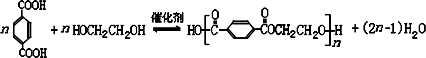
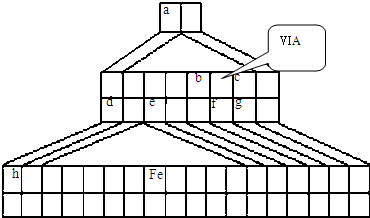
 NH3?H2O+H+
NH3?H2O+H+ (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.