题目内容
下列饱和溶液中通入过量CO2气体,肯定无沉淀生成的一组是( )
①NaOH ②Na2CO3 ③Na2SiO3 ④Ca(ClO)2 ⑤CaCl2.
①NaOH ②Na2CO3 ③Na2SiO3 ④Ca(ClO)2 ⑤CaCl2.
| A、①③ | B、②④ | C、②⑤ | D、④⑤ |
考点:钠的重要化合物,氯、溴、碘及其化合物的综合应用
专题:元素及其化合物
分析:向Ca(ClO)2溶液分别通入过量CO2,最终生成Ca(HCO3)2,没有沉淀生成;饱和NaOH、Na2CO3溶液中通入CO2,会析出NaHCO3晶体;饱和Na2SiO3溶液中通入CO2,会析出H2SiO3沉淀;CO2与CaCl2不反应,据此进行判断.
解答:
解:①饱和NaOH溶液中分别通入过量CO2,最终会析出NaHCO3晶体,有沉淀生成,故①错误;
②饱和Na2CO3溶液中通入CO2,会析出NaHCO3晶体,故②错误;
③饱和Na2SiO3溶液中通入CO2,会析出H2SiO3沉淀,故③错误;
④Ca(ClO)2溶液分别通入过量CO2,最终生成Ca(HCO3)2,没有沉淀生成,故④正确;
⑤CO2与CaCl2不反应,故⑤正确;
故选D.
②饱和Na2CO3溶液中通入CO2,会析出NaHCO3晶体,故②错误;
③饱和Na2SiO3溶液中通入CO2,会析出H2SiO3沉淀,故③错误;
④Ca(ClO)2溶液分别通入过量CO2,最终生成Ca(HCO3)2,没有沉淀生成,故④正确;
⑤CO2与CaCl2不反应,故⑤正确;
故选D.
点评:本题考查了离子反应发生条件、元素及其化合物的性质等,题目难度不大,注重了基础知识的考查,应该熟练掌握离子反应发生的条件.

练习册系列答案
相关题目
将CO2气体通入下列溶液中,无沉淀生成的是( )
| A、Na2SiO3溶液 |
| B、BaCl2溶液 |
| C、NaAlO2溶液 |
| D、硬脂酸钠溶液 |
下列物质都能导电,其中属于电解质的是( )
| A、熔融的NaOH | B、铁丝 |
| C、稀硫酸 | D、NaCl溶液 |
下列事实或现象与胶体性质无关的是( )
| A、一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通道 |
| B、明矾可以用来净水 |
| C、胶态金属氧化物分散于玻璃中制成有色玻璃 |
| D、三氯化铁溶液中加入NaOH溶液出现红褐色沉淀 |
 在一定条件下可实现如图所示物质之间的变化:
在一定条件下可实现如图所示物质之间的变化: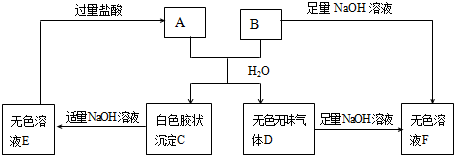
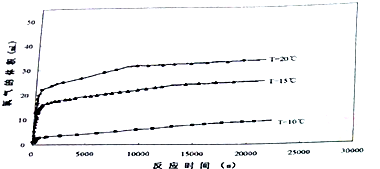 新型绿色硝化剂N205较传统硝化剂具有反应热效应小、温度容易控制、产物分离简单等优点,因而得到广泛的应用.
新型绿色硝化剂N205较传统硝化剂具有反应热效应小、温度容易控制、产物分离简单等优点,因而得到广泛的应用.