��Ŀ����
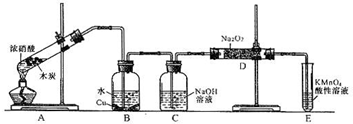
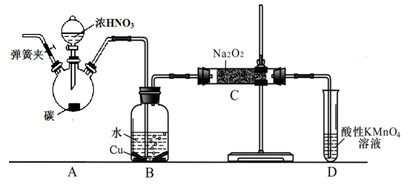
��12�֣�ij��ѧ��ȤС����̼��Ũ����Ϊ��ʼԭ�ϣ�������һ�Ȼ�����������Ʒ�Ӧ�Ʊ��������ơ����װ�����£�������װ���п�����Ӱ�죩

��ش��������⣺
��1��װ��A���Թ��з�����Ӧ�Ļ�ѧ����ʽ�� ��
��2���²�B�п��Թ۲����Ҫ������
��Cƿ������������ ��
��3����֪���������´��ڷ�Ӧ3HNO2=HNO3+2NO��+H2������������Һ�У�NO �ɽ�MnO
�ɽ�MnO ��ԭΪMn2+�����������ɡ�д������D�в������������Ƶķ�����
��ԭΪMn2+�����������ɡ�д������D�в������������Ƶķ�����
��
��4��Eװ�õ������� ��
��5��ͬѧ�Ǿ���������Ϊ����װ������ȱ�ݣ�Ϊ����D��������NaOH������ΪӦ�ý��еĸĽ��� ��
��1��C+4HNO3��Ũ�� CO2��+4NO2��+2H2O
CO2��+4NO2��+2H2O
��2����Һ������NO����һ����������
��3������I���������������Թ��У�����ϡ���ᣬ��������ɫ���岢��Һ���Ϸ���Ϊ����ɫ����D�в������������ơ���Ӧ�����ӷ���ʽ��3NO +2H+=NO
+2H+=NO +2NO��+H2O
+2NO��+H2O
����II���������������Թ��У���������KMnO4��Һ������Һ��ɫ��ȥ����D�в������������ƣ���Ӧ���뷽��ʽ��5 NO +2MnO
+2MnO +6H+=5 NO
+6H+=5 NO +2Mn2++3H2o�����������𰸾��÷֣�
+2Mn2++3H2o�����������𰸾��÷֣�
��4������D��δ��Ӧ���NO��������Ⱦ���������������𰸾��÷֣�
��5����C��D֮������һ��ʢŨ�����ϴ��ƿ����װ��ˮCaCl2�ĸ���ܣ������������𰸾��÷֣�
��������

 ��У����ϵ�д�
��У����ϵ�д�