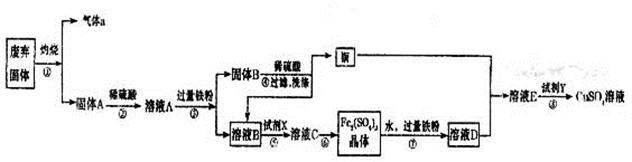
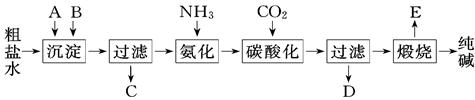
题目内容
铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某化学探究小组设计如下方案制备上述两种产品: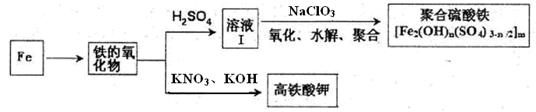
请回答下列问题:
(1)检验固体铁的氧化物中铁的化合价,应使用的试剂是 (填标号)
| A.稀硫酸 | B.稀硝酸 | C.KSCN溶液 | D.酸性高锰酸钾溶液 |
(3)Fe2O3与KNO3和KOH的混合物加热共融可制得高铁酸鉀。完成并配平下列化学方程式:
□Fe2O3+□KNO3+□KOH——□ +□KNO2+□ 。
(4)为测定溶液I中铁元素的总含量,实验操作:准确量取20.00mL溶液I于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用 0.1000mol·L—1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
已知:2Fe3++2I—=2Fe2++I2、I2+2S2O32—=2I—+S4O62—。
①写出滴定选用的指示剂 ,滴定终点观察到的现象 。
②溶液I中铁元素的总含量为 g·L—1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会 (填“偏高”、“偏低”、“不变”)。
(1)ACD(2分) (2)6Fe2++ClO3—+6H+=6Fe3++Cl—+3H2O(3分)
(3)1、3、4、2K2FeO4、3、2H2O(3分,写对生成物给1分)
(4)①淀粉(1分) 溶液由蓝色变无色且保持半分钟不变色(2分)
②5.6(2分) 偏高(1分)
解析试题分析:(1)铁的氧化物是碱性氧化物,能溶于稀硫酸和稀硝酸,但稀硝酸可以将Fe2+氧化为Fe3+,而稀硫酸则不能;Fe3+遇KSCN溶液变红,Fe2+可以使酸性高锰酸钾溶液褪色,故稀硫酸、KSCN溶液、酸性高锰酸钾溶液能检验氧化物中铁的化合价;(2)根据化合价升降相等、电荷守恒、原子守恒可得反应式6Fe2++ClO3—+6H+=6Fe3++Cl—+3H2O;(3)铁元素由+3价升为+6价,氮元素由+5价降为+3价,根据电子守恒、原子守恒可知,1Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O;(4)①淀粉遇I2变蓝,则滴定时指示剂为淀粉;当溶液由蓝色变为无色且半分钟内不变色时,即为滴定终点;②由c?V可知n(S2O32—)=0.1000mol/L×20.00×10—3L,由I2+2S2O32—=2I—+S4O62—可知n(I2)=n(S2O32—)/2=0.1000mol/L×20.00×10—3L÷2,由2Fe3++2I—=2Fe2++I2可知n(Fe3+)=2n(I2)=0.1000mol/L×20.00×10—3L÷2×2,由n?M可知m(Fe)=0.1000mol/L×20.00×10—3L÷2×2×56g/mol,则溶液I中铁元素的总含量为0.1000mol/L×20.00×10—3L÷2×2×56g/mol÷20.00×10—3L=5.6g·L—1;若滴定前H2O2没有除尽,则消耗硫代硫酸钠标准溶液的体积偏大,因此测定结果将偏高。
考点:考查铁及其化合物的性质、氧化还原反应方程式的配平、离子方程式的书写、滴定原理、指示剂、滴定终点、样品溶液中铁元素含量的测定等相关知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案在实验室里,某同学取一小块金属钠做与水反应的实验。试完成下列问题:
切开的金属钠暴露在空气中,最先观察到的现象是 ,所发生反应的化学方程式是 。
(2)将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是:
① ,② 。
将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是 (填编号)。
| A.有气体生成 | B.钠融化成小球并在液面上游动 |
| C.溶液底部有银白色的金属钙生成 | D.溶液变浑浊 |
(4)根据上述实验过程中钠所发生的有关变化,试说明将金属钠保存在煤油中的目的是 。
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,
回答下列问题:
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | ⑨ | ⑥ | ⑦ | | | ⑧ | |
(1)由①、②两种元素组成的相对分子质量为28的有机物的空间构型是 ,
该物质与溴水发生加成反应的化学方程式是 。
(2)用电子式表示④的简单氢化物的形成过程如下: ;
(3) 请设计实验比较元素⑥与⑨金属性的相对强弱: _;
(4) 用①元素的单质与④元素的单质可以制成电池,电池中装有KOH浓溶液,将多孔的惰性电极甲和乙浸入KOH溶液中,在甲极通入①的单质,乙极通入④的单质,则甲极的电极反应式为: 。
(5)由表中①、③、④、⑥、⑧元素形成的常见物质X、Y、Z、M、N可发生以下反应:
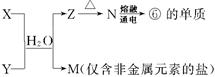
X溶液与Y溶液反应的离子方程式为 ,工业上常用单质⑥冶炼难熔的金属,写出氧化铁和单质⑥在高温下反应的化学方程式 。
(14分)
一位同学在复习时遇到这样一道习题:某无色溶液中可能含有“H+、OH-、Na+、NO3-”,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。
(1)加入铝粉产生H2,说明铝具有______(填“氧化性”或“还原性”)。
(2)该同学分析:若H+大量存在,则NO3-就不能大量存在。
设计实验证实如下:
| 装 置 | 现 象 |
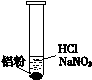 | ⅰ. 实验初始,未见明显现象 ⅱ. 过一会儿,出现气泡,液面上方呈浅棕色 ⅲ. 试管变热,溶液沸腾 |
① 盐酸溶解Al2O3薄膜的离子方程式是______。
② 根据现象ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
| 实 验 | 内 容 | 现 象 |
| 实验1 | 将湿润KI—淀粉试纸置于空气中 | 未变蓝 |
| 实验2 | 用湿润KI—淀粉试纸检验浅棕色气体 | 试纸变蓝 |
b. 实验1的目的是_______。
c. 实验1、2说明反应生成了NO,将生成NO的离子方程式补充完整:
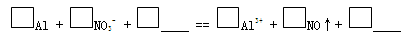
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在。
重新设计实验证实如下:
| 装 置 | 现 象 |
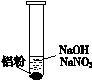 | ⅰ. 实验初始,未见明显现象 ⅱ. 过一会儿,出现气泡,有刺激性气味 |
为确认“刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
① 刺激性气味的气体是______。
② 产生该气体的离子方程式是______。
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是______。
(5)实验结果证实:NO3?在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物。习题中的无色溶液一定能大量存在的是Na+和OH-。
 4AlCl3+3O2 ↑。请回答下列问题:
4AlCl3+3O2 ↑。请回答下列问题: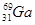 ,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。