题目内容
下列反应的离子方程式正确的是( )
| A、氯气通人含等物质的量的FeBr2溶液中:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 |
| B、澄清石灰水与少量的碳酸氢钠溶液反应:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
| C、铜与浓硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O |
| D、硫酸氢钠溶液滴入Ba(OH)2溶液至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.等物质的量反应,由电子守恒可知,亚铁离子全部氧化,而溴离子一半被氧化;
B.少量的碳酸氢钠完全反应,生成碳酸钙、水、NaOH;
C.反应生成二氧化氮;
D.至中性时以2:1反应,生成硫酸钡、硫酸钠、水.
B.少量的碳酸氢钠完全反应,生成碳酸钙、水、NaOH;
C.反应生成二氧化氮;
D.至中性时以2:1反应,生成硫酸钡、硫酸钠、水.
解答:
解:A.氯气通人含等物质的量的FeBr2溶液中的离子反应为2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2,故A正确;
B.澄清石灰水与少量的碳酸氢钠溶液反应的离子反应为Ca2++OH-+HCO3-=CaCO3↓+H2O,故B错误;
C.铜与浓硝酸反应的离子反应为Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,故C错误;
D.硫酸氢钠溶液滴入Ba(OH)2溶液至中性的离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D错误;
故选A
B.澄清石灰水与少量的碳酸氢钠溶液反应的离子反应为Ca2++OH-+HCO3-=CaCO3↓+H2O,故B错误;
C.铜与浓硝酸反应的离子反应为Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,故C错误;
D.硫酸氢钠溶液滴入Ba(OH)2溶液至中性的离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D错误;
故选A
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关离子反应的考查,注意电子、电荷守恒的应用,题目难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、滴人酚酞溶液显红色的溶液中:K+、Na+、Cu2+、SO42- |
| B、能使红色石蕊试纸变蓝色的溶液中:K+、CO32-、NO3-、AlO2- |
| C、水电离产生的.(H+)=10-13mol/L的溶液中:Na+、Cl-、NO3-、CH3 COO- |
| D、pH=l 的溶液中:Na+、Fe2+、NO3-、Cl- |
用化学方法区别SO2与CO2最好选用的化学试剂是( )
| A、紫色的石蕊试液 |
| B、品红溶液 |
| C、澄清的石灰水 |
| D、氢氧化钠溶液 |
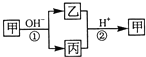 甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
甲是一种常见的单质,乙、丙为中学常见的化合物,甲、乙、丙均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )| A、X元素可能为Al |
| B、X 元素不一定为非金属元素 |
| C、反应①和②互为可逆反应 |
| D、反应①和②一定为氧化还原反应 |
由1-丙醇制取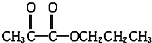 ,最简便的流程需要下列反应的顺序应是( )
,最简便的流程需要下列反应的顺序应是( )
a.氧化 b.还原 c.取代 d.加成 e.消去 f.中和 g.加聚 h.酯化.
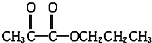 ,最简便的流程需要下列反应的顺序应是( )
,最简便的流程需要下列反应的顺序应是( )a.氧化 b.还原 c.取代 d.加成 e.消去 f.中和 g.加聚 h.酯化.
| A、e、d、c、a、h |
| B、b、d、f、g、h |
| C、a、e、d、c、h |
| D、b、a、e、c、f |
下列各组物质,不用任何化学试剂即可鉴别的是( )
| A、氯水、NaBr溶液、盐酸 |
| B、NaCl溶液、NaBr溶液、KI溶液 |
| C、氯化氢、溴化氢、碘化氢 |
| D、盐酸、NaCl溶液、AgNO3溶液、Na2CO3溶液 |
下列装置或操作能达到实验目的是( )
A、 除去乙醇中的乙酸 |
B、 形成原电池 |
C、 制取乙酸乙酯 |
D、 甲烷的取代反应 |
下列各组中的物质或离子都含配位键的是( )
| A、H2O、Al2Cl6 |
| B、CO2、SO42- |
| C、H3O+、[Cu(NH3)4]SO4 |
| D、NH4Cl、C2H2 |
 一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )
一定条件下,下列反应可为工业制盐酸、合成氨提供原料:CH4 (g)+H2O (g)?CO(g)+3H2(g)△H>0.当该反应达到平衡后,若仅改变图中x的量,重新达到平衡后,y值随x变化趋势合理的是( )