题目内容
 在一定温度下,向容积不变的容器中加入2mol N2、8mol H2及固体催化剂,使之反应.已知:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ?mol-1.平衡时,容器内气体压强为起始时的80%.
在一定温度下,向容积不变的容器中加入2mol N2、8mol H2及固体催化剂,使之反应.已知:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ?mol-1.平衡时,容器内气体压强为起始时的80%.(1)反应达到平衡时,放出的热量
A.小于92.2kJ B.等于92.2kJ C.大于92.2kJ
(2)欲使H2的转化率提高为原来的两倍,则在其他条件不变的情况下,应将N2的初始量由2mol提高至
(3)保持同一温度,在相同的容器中,若起始时加入2molNH3、1molH2及固体催化剂,反应达到平衡时NH3的体积分数
A.等于0.25 B.大于0.25 C.小于0.25
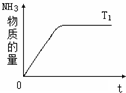
(4)右图是T1℃时容器中NH3的物质的量随时间的变化曲线,请在该图中补画出该反应在T2℃(T2>T1)时n(NH3)的变化曲线.
考点:化学平衡的影响因素,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)根据反应:N2(g)+3H2(g)?2NH3(g),利用三段式计算;
(2)依据平衡常数计算分析;
(3)将氨气按反应转化为反应物,则相当于起始量为1molN2和4molH2,相当于上述起始量的一半,从压强对平衡的影响角度分析;
(4)由于T2>T1,平衡向逆反应方向移动,平衡时NH3的百分含量减小,但温度升高,速率增大,以此判断.
(2)依据平衡常数计算分析;
(3)将氨气按反应转化为反应物,则相当于起始量为1molN2和4molH2,相当于上述起始量的一半,从压强对平衡的影响角度分析;
(4)由于T2>T1,平衡向逆反应方向移动,平衡时NH3的百分含量减小,但温度升高,速率增大,以此判断.
解答:
解:(1)利用三段式计算:
N2(g)+3H2(g)?2NH3(g)
起始:2mol 8mol 0
转化:x 3x 2x
平衡:2-x 8-3x 2x
根据压强之比等于物质的量之比,则有:(2-x+6-3x+2x)÷(2+8)=0.8,解之得x=1,
则NH3的物质的量为2mol,则NH3的体积分数为
×100%=25%,
由热化学反应方程式可知此时反应的氮气为1mol,所以放出的热量等于92.2kJ,
故答案为:B;
(2)达平衡时,N2、H2、NH3的量分别为1molN2、5molH2、2molNH3,欲使H2的转化率提高为原来的两倍,氢气转化率为
×2,消耗氢气物质的量为6mol,则在其他条件不变的情况下,消耗氮气物质的量为2mol,平衡后氢气为2mol,氮气为(X-2)mol,生成氨气物质的量为4mol,应将N2的初始量由2mol提高至X,设体积为1L,则依据平衡常数不变得到:
=
X=64.5
故答案为:64.5;
(3)将氨气按反应转化为反应物,则相当于起始量为1molN2和4molH2,相当于上述起始量的一半,则压强是原来的一半,压强减小,平衡向逆反应方向移动,NH3的百分含量减小,即小于25%,故答案为:C;
(4)由于T2>T1,平衡向逆反应方向移动,平衡时NH3的百分含量减小,但温度升高,速率增大,达到平衡的时间缩短,故图象为 ,故答案为:
,故答案为: .
.
N2(g)+3H2(g)?2NH3(g)
起始:2mol 8mol 0
转化:x 3x 2x
平衡:2-x 8-3x 2x
根据压强之比等于物质的量之比,则有:(2-x+6-3x+2x)÷(2+8)=0.8,解之得x=1,
则NH3的物质的量为2mol,则NH3的体积分数为
| 2x |
| (2-x+8-3x+2x) |
由热化学反应方程式可知此时反应的氮气为1mol,所以放出的热量等于92.2kJ,
故答案为:B;
(2)达平衡时,N2、H2、NH3的量分别为1molN2、5molH2、2molNH3,欲使H2的转化率提高为原来的两倍,氢气转化率为
| 3 |
| 8 |
| 22 |
| 1×52 |
| 42 |
| (X-2)×23 |
X=64.5
故答案为:64.5;
(3)将氨气按反应转化为反应物,则相当于起始量为1molN2和4molH2,相当于上述起始量的一半,则压强是原来的一半,压强减小,平衡向逆反应方向移动,NH3的百分含量减小,即小于25%,故答案为:C;
(4)由于T2>T1,平衡向逆反应方向移动,平衡时NH3的百分含量减小,但温度升高,速率增大,达到平衡的时间缩短,故图象为
 ,故答案为:
,故答案为: .
.
点评:本体考查化学平衡移动问题,题目难度较大,注意(1)(2)为易错点,注意化学平衡计算的方法,特别是(2)注意从平衡常数的角度分析计算.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、向氢氧化钡溶液中加硫酸溶液:Ba2++SO42-=BaSO4↓ | ||||
| B、通常情况下铁与稀硝酸反应:Fe+2H+=Fe2++H2↑ | ||||
C、二氧化锰与浓盐酸共热:MnO2+4 HCl (浓)
| ||||
| D、碳酸氢钠溶液中加入少量的澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、
等已被发现.下列有关说法中正确的是( )
| N | + 5 |
| A、C60的相对分子质量为720g/mol | ||
| B、H2与H3属于同素异形体 | ||
| C、O2与O4属于同位素 | ||
D、
|
在下列过程中,需要加快化学反应速率的是( )
| A、塑料老化 | B、炼钢 |
| C、钢铁生锈 | D、食物腐败 |
乙烯能够在一定条件下与下列物质发生化学反应的是( )
①水 ②氢气 ③溴水 ④乙烯 ⑤与氯化氢 ⑥酸性高锰酸钾.
①水 ②氢气 ③溴水 ④乙烯 ⑤与氯化氢 ⑥酸性高锰酸钾.
| A、全部 | B、②③⑤ |
| C、①③⑤⑥ | D、②③⑤⑥ |
在某密闭恒容容器中存在下列化学平衡:aA(气)?bB(气)+cC(气),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是( )
| A、若 a=b+c,B的物质的量分数变大 |
| B、若 a>b+c,B 的物质的量分数减小 |
| C、若a>b+c时,A的转化率不变 |
| D、若a<b+c时,A的转化率变小 |
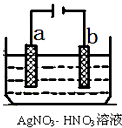 按要求完成下列问题:
按要求完成下列问题: