题目内容
15.将8g NaOH溶解在水中,要使Na+与H2O数之比为1:100,需水20mol,其溶液中有0.2mol NaOH,中和这些NaOH,需2mol/L的HCl100mL,或者需要9.8g的硫酸.分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$结合反应的化学方程式NaOH+HCl=NaCl+H2O、2NaOH+H2SO4=Na2SO4+2H2O计算.
解答 解:n(NaOH)=$\frac{8g}{40g/mol}$=0.2mol,要使Na+与H2O数之比为1:100,则n(H2O)=20mol,与盐酸反应的方程式为NaOH+HCl=NaCl+H2O,可知盐酸溶液的体积为$\frac{0.2mol}{2mol/L}$=0.1L=100mL,由方程式2NaOH+H2SO4=Na2SO4+2H2O可知需要0.1mol硫酸,质量为0.1mol×98g/mol=9.8g,
故答案为:20;0.2;100;9.8.
点评 本题综合考查物质的量的计算,为高频考点,侧重于学生的分析能力的考查,注意把握相关计算公式的运用,结合方程式计算该题,难度不大.

练习册系列答案
相关题目
5.下列离子方程式正确的是( )
| A. | 苯酚与碳酸氢钠溶液反应:C6H5OH+HCO3-→C6H5O-+CO2↑+H2O | |
| B. | 溴乙烷转化成乙醇:C2H5Br+OH- $→_{△}^{水}$C2H5OH+Br- | |
| C. | 肥皂液加入醋酸:C17H35COO-+H+→C17H35COOH | |
| D. | 甲醛溶液与足量的新制Cu(OH)2共热:HCHO+2Cu(OH)2+OH-$\stackrel{△}{→}$HCOO-+Cu2O↓+3H2O |
3.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,1 mol CO2、CO的混合气中含有的氧原子数为1.5NA | |
| B. | 常温常压下,11.2 L 氯化氢气体中含有的分子数为0.5NA | |
| C. | NA个甲烷分子和1mol甲烷的质量相等 | |
| D. | 1 mol•L-1 CuCl2溶液中含有的氯离子数为2NA |
10.下列关于物质性质或检验的叙述正确的是( )
| A. | 在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ | |
| B. | 气体通过湿润的蓝色石蕊试纸,试纸变红,证明原气体中含有氨气 | |
| C. | 用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,可能有K+ | |
| D. | 将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2 |
7.下列物质中所含原子数最多的是( )
| A. | 6.02×1023个N2 | B. | 9g H2O | C. | 0.5mol Br2 | D. | 10g H2 |
4.Mg、Al、Fe分别与足量的HC1反应,产生的气体在相同状况下,均是5.6升,则Mg、Al、Fe三种金属物质的量比为( )
| A. | 3:2:2 | B. | 2:3:2 | C. | 2:2:3 | D. | 3:2:3 |

 如图装置中,U型管内为红墨水,a,b试管内分别盛有是食盐水和醋酸溶液,各加入生铁快,放置右方时间,请回答下列问题:
如图装置中,U型管内为红墨水,a,b试管内分别盛有是食盐水和醋酸溶液,各加入生铁快,放置右方时间,请回答下列问题: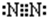 ,其中的化学键属于共价键(填“离子”或“共价”).
,其中的化学键属于共价键(填“离子”或“共价”).