题目内容
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。
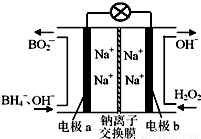
下列说法正确的是
A.电池放电时Na+从a极区移向b极区
B.每消耗3 mol H2O2,转移的电子为3 mol
C.电极a采用MnO2,MnO2既作电极材料又有催化作用
D.该电池的负极反应为:BH4-+2H2O-8e-=== BO2-+8H+
A
【解析】
试题分析:A、在原电池中负极失去电子,正极得到电子,阳离子向正极移动,阴离子向负极移动。b电极是双氧水放电,因此b电极是正极,a电极是负极,则Na+从a极区移向b极区,A正确;B、双氧水在正极放电,电极反应式为H2O2+2e-=2OH-,每消耗3molH2O2,转移6mol电子,B错误;C、电极b是正极,采用MnO2,H2O2发生还原反应,得到电子被还原生成OH-,MnO2既作电极材料又有催化作用,C错误;D、负极失去电子,发生氧化反应生成BO2-,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,D错误,答案选A。
考点:考查原电池原理的应用

 名校课堂系列答案
名校课堂系列答案下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向两份蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4 溶液 | 均有固体析出 | 蛋白质均发生变性 |
B | 向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X 中一定含有SO42- |
C | 用大理石和盐酸反应制取CO2 气体,立即通入一定浓度的Na2SiO3 溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
D | 向浓度均为0. 1 mol·L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3 溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
已知草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂。
(1)草酸的电离方程式为 。
(2)将草酸溶液与酸性高锰酸钾溶液混合发生的反应为:
MnO4-+ H2C2O4+ → Mn2+ + CO2↑+ H2O
某合作小组同学在烧杯中进行上述反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
①配平上述离子方程式
②该实验不久后溶液突然褪色的原因最有可能是 。
A.体系压强增大 B.反应物接触面积增大
C.生成物对反应有催化作用 D.反应物浓度增大
(3)为研究该化学反应速率的影响因素,某同学进行了以下实验:
组别 | 温度/℃ | V(H2C2O4) /mL | V(KMnO4) /mL | V(H2O) /mL | KMnO4溶液 褪色时间/s |
1 | 30 | 10 | 10 | 20 | 40 |
2 | 30 | 20 | 20 | 0 | t |
3 | 30 |
|
| 15 |
①对比实验1和3要研究改变反应物浓度对化学反应速率的影响,请完成表格中横线。
②实验2中溶液褪色时间t 为
A.>40 B.=40 C.<40 D.无法判断

 NaBC2+NaBC + H2O
NaBC2+NaBC + H2O





