题目内容
现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了确定四种溶液各是什么,将它们随意编上A、B、C、D后,产生的现象如下表所示.根据实验现象回答
(1)写出B+D反应的离子方程式
(2)写出A+D反应的离子方程式 .
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有现象发生 |
| ② | B+D | 有气体放出 |
| ③ | B+C | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
(2)写出A+D反应的离子方程式
考点:离子方程式的书写
专题:离子反应专题
分析:B和D有气体生成,只有碳酸钠和盐酸反应能生成气体,所以B和D是盐酸和碳酸钠,A和C是氯化钙和硝酸银;A和B 没有现象发生,所以B是盐酸,A是氯化钙,D是碳酸钠,C是硝酸银,
(1)盐酸和碳酸钠反应生成氯化钠和二氧化碳、水;
(2)氯化钙和碳酸钠反应生成碳酸钙和氯化钠.
(1)盐酸和碳酸钠反应生成氯化钠和二氧化碳、水;
(2)氯化钙和碳酸钠反应生成碳酸钙和氯化钠.
解答:
解:B和D有气体生成,只有碳酸钠和盐酸反应能生成气体,所以B和D是盐酸和碳酸钠,A和C是氯化钙和硝酸银;A和B 没有现象发生,所以B是盐酸,A是氯化钙,D是碳酸钠,C是硝酸银,
(1)盐酸和碳酸钠反应生成氯化钠和二氧化碳、水,离子方程式为2H++CO32-=H2O+CO2↑,故答案为:2H++CO32-=H2O+CO2↑;
(2)氯化钙和碳酸钠反应生成碳酸钙和氯化钠,离子方程式为Ca2++CO32-=CaCO3↓,故答案为:Ca2++CO32-=CaCO3↓.
(1)盐酸和碳酸钠反应生成氯化钠和二氧化碳、水,离子方程式为2H++CO32-=H2O+CO2↑,故答案为:2H++CO32-=H2O+CO2↑;
(2)氯化钙和碳酸钠反应生成碳酸钙和氯化钠,离子方程式为Ca2++CO32-=CaCO3↓,故答案为:Ca2++CO32-=CaCO3↓.
点评:本题考查了离子方程式的书写,为高考高频点,明确物质的性质及离子方程式书写规则是解本题关键,知道常见物质的溶解性,题目难度不大.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
下列变化需要加入还原剂才能实现的是( )
| A、CO32-→CO2 |
| B、Cu→Cu2+ |
| C、Na→Na+ |
| D、KMnO4→MnCl2 |
NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、2.4g镁与足量的盐酸反应,电子转移数目为0.1NA |
| B、0.5mol/L的Na2SO4的溶液中含NA个Na+ |
| C、1molNa2O2固体中含2NA个阴离子 |
| D、1molCH5+离子所含电子数为10NA |
下列有关化学用语表示正确的是( )
A、3,3-二甲基-1-戊烯的键线式: |
B、甲醛的电子式: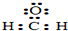 |
C、乙醇分子的比例模型: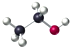 |
D、CH4Si的结构式: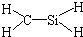 |
下列实验操作中,所用试剂正确的是( )
| A、用酒精萃取碘水中的碘 |
| B、用氯化钡溶液鉴别稀盐酸和稀硫酸 |
| C、用稀硫酸洗去残留在试管壁上的碳酸钙 |
| D、用稀盐酸鉴别碳酸钠溶液和碳酸钾溶液 |
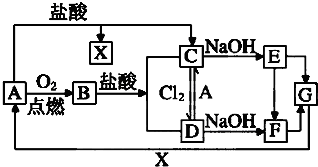 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题. X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.