题目内容
下列家庭化学小实验不能达到预期目的是( )
| A、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| B、用燃烧法检验衣服面料是羊毛还是化学纤维 |
| C、用分液法分离水和油 |
| D、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验? |
考点:有机物的鉴别,分液和萃取,蛋白质的盐析
专题:
分析:A、淀粉遇单质碘变蓝;
B、羊毛含有蛋白质,灼烧有烧焦羽毛的气味;
C、水和油会分层;
D、蛋白质难溶于饱和食盐水.
B、羊毛含有蛋白质,灼烧有烧焦羽毛的气味;
C、水和油会分层;
D、蛋白质难溶于饱和食盐水.
解答:
解:A、淀粉遇单质碘变蓝,而食用加碘盐为KIO3,不能用来检验,故A错误;
B、羊毛含有蛋白质,灼烧有烧焦羽毛的气味,化学纤维灼烧没有烧焦羽毛的气味,所以可以用燃烧法检验衣服面料是羊毛还是化学纤维,故B正确;
C、水和油互不相溶,会分层,可以用分液法分离,故C正确;
D、蛋白质难溶于饱和食盐水,属于盐析现象,为可逆过程,加水后能重新溶解,故D正确.
故选A.
B、羊毛含有蛋白质,灼烧有烧焦羽毛的气味,化学纤维灼烧没有烧焦羽毛的气味,所以可以用燃烧法检验衣服面料是羊毛还是化学纤维,故B正确;
C、水和油互不相溶,会分层,可以用分液法分离,故C正确;
D、蛋白质难溶于饱和食盐水,属于盐析现象,为可逆过程,加水后能重新溶解,故D正确.
故选A.
点评:本题考查物质的检验和鉴别,题目难度不大,本题注意碘盐的组成、注意蛋白质的性质.

练习册系列答案
相关题目
下列实验装置能达到相应实验目的是( )
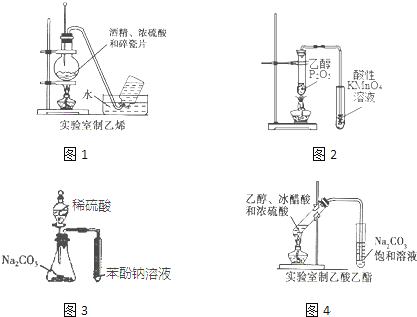

| A、图1装置一定可以制得乙烯 |
| B、图2装置可以证明CH3CH2OH发生消去反应生成了乙烯 |
| C、图3所示装置可以证明碳酸酸性强于苯酚 |
| D、实验室常用图4所示装置制取少量的乙酸乙酯 (夹持物略) |
下列实验的相关描述正确的是( )
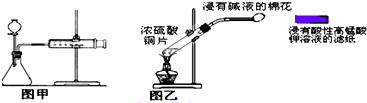

| A、快速分离氢氧化铁胶状沉淀和氯化钠溶液可用抽滤法 |
| B、常温下,苯酚与水形成的浊液静置后会分层,上层为溶有水的苯酚溶液 |
| C、甲装置可用于某些化学反应速率的测定.该装置气密性的检查如下:仪器组装好后,关闭分液漏斗活塞,将针筒活塞向外拉一段距离,然后松手,观察针筒是否能回到原来刻度处 |
| D、乙装置可用来制取和检验二氧化硫气体漂白性,待滤纸颜色褪去后立即用浸有碱液的棉花堵住试管口 |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.下列说法不正确的是( )
| A、淀粉和纤维素均可用(C6H10O5)n表示 |
| B、淀粉水解的最终产物能发生银境反应 |
| C、向蛋白质溶液中加入饱和硫酸铵溶液后产生的沉淀能重新溶于水 |
| D、脂肪能溶于水 |
胡椒酚是植物挥发油的成分之一,它的结构简式为:HO- -CH2CH=CH2,下列叙述中正确的是( )
-CH2CH=CH2,下列叙述中正确的是( )
 -CH2CH=CH2,下列叙述中正确的是( )
-CH2CH=CH2,下列叙述中正确的是( )| A、1mol胡椒酚最多可与4molH2发生反应 |
| B、1mol胡椒酚最多可与4mol溴发生反应 |
| C、胡椒酚中所有原子可以共平面 |
| D、胡椒酚在水中的溶解度小于苯酚在水中的溶解度 |
下列关于金属钠的叙述错误的是( )
| A、金属钠可以保存在煤油中 |
| B、金属钠着火时,可用泡沫灭火器来灭火 |
| C、钠与熔融的四氯化钛反应可制取钛 |
| D、实验时用剩的钠块应该放回原试剂瓶 |
下列各组离子中,因相互促进水解,而不能大量共存的是( )
| A、Al3+、SO42-、CO32-、Cl- |
| B、Na+、HCO3-、AlO2-、Cl- |
| C、H+、HS-、Na+、SO32- |
| D、OH-、Na+、K+、HCO3- |