题目内容
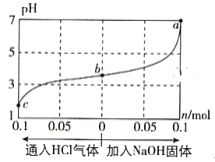
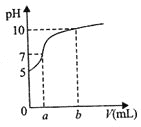
【题目】常温下,用石墨电极电解100mL、0.1molL-1NH4Cl溶液,电解过程中溶液体积变化忽略不计,溶液的pH随阳极产生气体体积(标准状况下)变化的曲线如图,下列说法正确的是( )
A.溶液pH=5时,c(NH3H2O)=1.0×10-5molL-1
B.电解过程使NH4+的水解程度减小,pH增大
C.若b=56mL,c(NH4+)≈5.01×10-2molL-1
D.若将阳极产生的bmL气体重新通回溶液,c(NH4+)不会改变
【答案】C
【解析】
用惰性材料作电极,电解NH4Cl溶液,根据电解原理,阳极反应式为2Cl--2e-=Cl2↑、2H2O-4e-=O2↑+4H+,阴极反应式为2H2O+2e-=H2↑+2OH-,据此分析;
A. 溶液的![]() 时,溶质只有NH4Cl,溶液中的
时,溶质只有NH4Cl,溶液中的![]() ,由于溶液中氢离子浓度包括水电离出的H+和NH4+水解产生的H+,则由
,由于溶液中氢离子浓度包括水电离出的H+和NH4+水解产生的H+,则由![]() ,可知
,可知![]() 略小于
略小于![]() ,故A说法错误;
,故A说法错误;
B. 由图可知,电解过程中,阴极是氢离子放电,使铵根离子的水解平衡正向移动,铵根离子的水解程度加大,故B说法错误;
C. 若氯气为56mL,则溶液中的![]() ,
,![]() ,由溶液中电荷守恒可知,
,由溶液中电荷守恒可知,![]() ,则
,则![]() ,故C说法正确;
,故C说法正确;
D. 电解过程中,阴极产生氢气,阳极产生氯气,若将阳极产生的bmL氯气重新通回溶液,溶液不能回复到原来的状态,![]() 会改变,故D说法错误。
会改变,故D说法错误。
答案:C。

练习册系列答案
相关题目