题目内容
(14分)(1)下图是工业氮气和氢气合成1mol氨气过程中能量变化示意图,

请写出该反应的热化学方程式 。
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=C02(g) △H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599kJ·mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变:△H=____ 。
(3)将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如下图所示。

正极上发生的电极反应为___
阴极上发生的电极反应为___
(4)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是________(填“a”或“b”)极,负极的电极反应式是 __ _。
②电池工作一段时间后电解质溶液的pH______(填“增大”、“减小”或“不变”)
(1)N2(g)+3H2 (g)===2NH3(g) ΔH=2(a-b)kJ/mol
(2)226.7kJ·mol-1 (3) 2H2O+O2 +4e-==4OH- 2H++2e-==H2↑
(4)①a CH4+10OH-―8e-=CO32-+7H2O ②减小
【解析】
试题分析:(1)①由图1可知,1molN2(g)与3molH2(g)完全反应生成2molNH3(g)的反应热为508kJ/mol-600kJ/mol=-92kJ/mol,所以合成氨的热化学反应方程式为:N2(g)+3H2 (g)2NH3(g)△H=-92kJ/mol,故答案为:N2(g)+3H2(g)
(g)2NH3(g)△H=-92kJ/mol,故答案为:N2(g)+3H2(g) 2NH3(g)△H=-92kJ/mol。
2NH3(g)△H=-92kJ/mol。
(2)已知:①C (s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ?mol-1;
②2H2(g)+O2(g)=2H2O (l)△H2=-571.6kJ?mol-1;
③2C2H2(g)+5O2(g)═4CO2(g)+2H2O (l)△H2=-2599kJ?mol-1;
2C (s,石墨)+H2(g)=C2H2(g)的反应可以根据①×2+②×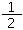 -③×
-③×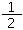 得到,所以反应焓变△H=2×(-393.5kJ?mol-1)+(-571.6kJ?mol-1)×
得到,所以反应焓变△H=2×(-393.5kJ?mol-1)+(-571.6kJ?mol-1)×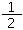 -(-2599kJ?mol-1)×
-(-2599kJ?mol-1)×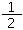 =+226.7kJ?mol-1,故答案为:△H=+226.7kJ?mol-1.
=+226.7kJ?mol-1,故答案为:△H=+226.7kJ?mol-1.
(3) 甲图示是原电池,锌做负极,锌失电子形成锌离子,正极是Ⅰ,在正极上,O2+2H2O+4e-=4OH-;所以Ⅰ处变红;乙图示是电解池,铁做阳极,铁失电子生成亚铁离子,锌做阴极,在阴极上,2H++2e-=H2↑,破坏了锌片附近水的电离平衡,使得OH-浓度增大,所以Ⅳ处也变红.故答案为:2H2O+O2 +4e-==4OH- 2H++2e-==H2↑
(4)由原电池原理确定a极为负极,电极反应式为CH4+10OH--8e-==CO32-+7H2O;正极反应式为2O2+4H2O+8e-==8OH-;合并的原电池的总反应式为CH4+2OH-+2O2==3H2O+ CO32-;确定工作一段时间后溶液的p H会减小;故答案为:①a CH4+10OH-―8e-=CO32-+7H2O ②减小
考点:热化学方程式的书写、盖斯定律的应用、原电池和电解池的工作原理、简单实验及p H的计算。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案 mol·L-1
mol·L-1 mol·L-1
mol·L-1 mol·L-1
mol·L-1 mol·L-1
mol·L-1 H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是 xC(g),达到平衡时测得 A的浓度为 0.5 mol/L,在温度不变的条件下,将容器的容积扩大到原来的2倍, 再达平衡时测得A的浓度为 0.3 mol/L ,下列有关判断正确的是
xC(g),达到平衡时测得 A的浓度为 0.5 mol/L,在温度不变的条件下,将容器的容积扩大到原来的2倍, 再达平衡时测得A的浓度为 0.3 mol/L ,下列有关判断正确的是