题目内容
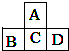 A、B、C、D为短周期元素,它们的位置关系如图所示,已知B、D两元素原子序数之和是A元素的原子序数的4倍,则下列叙述中正确的是( )
A、B、C、D为短周期元素,它们的位置关系如图所示,已知B、D两元素原子序数之和是A元素的原子序数的4倍,则下列叙述中正确的是( )分析:A、B、C、D为短周期元素,由位置可知,A为第二周期元素,B、C、D为第三周期元素,设A的原子序数为x,则B、C、D的原子序数分别为x+7、x+8、x+9,由B、D两元素原子序数之和是A元素的原子序数的4倍,则x+7+x+9=4x,解得x=8,则A为O,B为P,C为S,D为Cl,然后结合物质的性质及元素周期律来解答.
解答:解:A、B、C、D为短周期元素,由位置可知,A为第二周期元素,B、C、D为第三周期元素,设A的原子序数为x,则B、C、D的原子序数分别为x+7、x+8、x+9,由B、D两元素原子序数之和是A元素的原子序数的4倍,则x+7+x+9=4x,解得x=8,则A为O,B为P,C为S,D为Cl,
A.非金属性D>C,则C的最高价氧化物对应水化物的酸性比D的弱,故A错误;
B.非金属性A>C,则A的气态氢化物比C的稳定,故B正确;
C.同周期从左向右非金属性增强,则B的非金属性比C的弱,故C错误;
D.C在足量的A2中燃烧的产物是C2A(为H2S),故D错误;
故选B.
A.非金属性D>C,则C的最高价氧化物对应水化物的酸性比D的弱,故A错误;
B.非金属性A>C,则A的气态氢化物比C的稳定,故B正确;
C.同周期从左向右非金属性增强,则B的非金属性比C的弱,故C错误;
D.C在足量的A2中燃烧的产物是C2A(为H2S),故D错误;
故选B.
点评:本题考查位置、结构、性质的关系,明确图中的位置得出原子序数的关系是解答本题的关键,注意把握元素周期律及非金属性的关系即可解答,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
【化学一选修3:物质结构与性质】(15分)
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
形
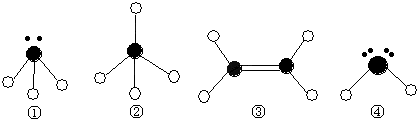
(2)某同学根据上述信息,所画的B电子排布图如图

违背了 原理。
(3)F位于 族 区,其基态原子有 种运动状态。
(4)CD3 中心原子的杂化方式为 ,用价层电子对互斥理论推测其分子空间构型为 .检验E元素的方法是
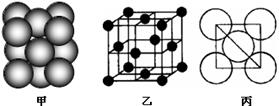
(5)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为 ,该单质晶体中原子的堆积方式为四种基本堆积方式中的 .
【化学一选修3:物质结构与性质】(15分)
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
|
A元素原子的核外p电子总数比s电子总数少1 |
|
B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
|
C原子核外所有p轨道全满或半满 |
|
D元素的主族序数与周期数的差为4 |
|
E是前四周期中电负性最小的元素 |
|
F在周期表的第七列 |
(1)A基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈
形
(2)某同学根据上述信息,所画的B电子排布图如图
违背了 原理。
(3)F位于 族 区,其基态原子有 种运动状态。
(4)CD3 中心原子的杂化方式为 ,用价层电子对互斥理论推测其分子空间构型为 .检验E元素的方法是
(5)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为 ,该单质晶体中原子的堆积方式为四种基本堆积方式中的 .


 ,违背了 原理。
,违背了 原理。