题目内容
 将一定量的镁铝合金放入一定量的盐酸中,合金恰好全部溶解,向所得溶液中滴加一定浓度的NaOH溶液,加入的NaOH溶液的体积(V)与沉淀质量(m)的关系如图所示.下面说法正确的是( )
将一定量的镁铝合金放入一定量的盐酸中,合金恰好全部溶解,向所得溶液中滴加一定浓度的NaOH溶液,加入的NaOH溶液的体积(V)与沉淀质量(m)的关系如图所示.下面说法正确的是( )| A、A点的沉淀是Mg (OH)2、Al (OH)3 |
| B、B点的沉淀是Mg (OH)2、Al (OH)3 |
| C、A点时溶液中的溶质有NaCl和NaAlO2 |
| D、B点时溶液中的溶质只有NaCl和NaAlO2 |
考点:铝的化学性质,镁的化学性质
专题:元素及其化合物
分析:由图可知,盐酸没有剩余,A点之前发生氯化铝、氯化镁与NaOH的反应,A点沉淀最多;A→B发生Al(OH)3+NaOH=NaAlO2+2H2O,则B点沉淀只有Mg(OH)2,以此来解答.
解答:
解:由图可知,盐酸没有剩余,A点之前发生氯化铝、氯化镁与NaOH的反应,A点沉淀最多,A点的沉淀是Mg (OH)2、Al(OH)3,溶质只有NaCl;
A→B发生Al(OH)3+NaOH=NaAlO2+2H2O,则B点沉淀只有Mg(OH)2,则溶质为NaCl和NaAlO2,
故选AD.
A→B发生Al(OH)3+NaOH=NaAlO2+2H2O,则B点沉淀只有Mg(OH)2,则溶质为NaCl和NaAlO2,
故选AD.
点评:本题考查镁、铝的性质,为高频考点,侧重于分析能力的考查,把握图中点、线的意义及发生的反应为解答的关键,注意金属及其化合物是重要的无机物,是历年高考的重点,学生在备考过程中应注意积累各物质的性质及重要的化学反应.

练习册系列答案
相关题目
氢化钠是一种离子化合物,它跟水反应时生成氢氧化钠和氢气,反应方程式为NaH+H2O═NaOH+H2↑,将氢化钠和铝粉的混合物mg与足量的水充分反应后,若收集到ng氢气,则混合物中的铝的质量为( )
| A、(36n-3m)g |
| B、(m-4.8n)g |
| C、(12n-m)g |
| D、(24m-5n)g |
在玻璃、水泥和高炉炼铁工业生产中,都需要的原料是( )
| A、石灰石 | B、纯碱 | C、粘土 | D、石英 |
下列说法不正确的是( )
| A、热的纯碱液去油污效果好,因为加热可使CO32-的水解程度增大,溶液碱性增强,去污力增强 | ||||
| B、铁在潮湿的环境下生锈以及Mg与NH4Cl溶液反应生成H2都与盐类水解有关 | ||||
| C、将Al2(SO4)3溶液加热、蒸干、灼烧,可得到固体Al2(SO4)3 | ||||
D、将饱和FeCl3溶液滴入沸水中制胶体,离子方程式:Fe3++3H2O
|
将钠放置在空气中,是生成白色的Na2O还是淡黄色的Na2O2,主要取决于下列因素中的( )
| A、反应温度 | B、空气的量 |
| C、钠粒的大小 | D、钠的形状 |
下列物质中,属于醇类的是( )
| A、CH3OCH3 |
| B、CH3CHO |
| C、CH3COOH |
| D、CH3CH2OH |
已知:Fe2O3(s)+
C(s)═
CO2(g)+2Fe(s)△H=+234.1kJ/mol
C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
则:2Fe(s)+
O2(g)═Fe2O3(s)的△H是( )
| 3 |
| 2 |
| 3 |
| 2 |
C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
则:2Fe(s)+
| 3 |
| 2 |
| A、-824.4 kJ/mol |
| B、-627.6 kJ/mol |
| C、-744.7 kJ/mol |
| D、-169.4 kJ/mol |
下列化学用语的书写,不正确的是( )
| A、葡萄糖的分子式:C6H12O6 |
| B、氯气的电子式:Cl:Cl |
| C、乙醇的结构简式:CH3CH2OH |
D、硫原子的结构示意图: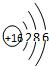 |
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )


| A、属于芳香烃 |
| B、属于卤代烃 |
| C、该有机物有四种官能团 |
| D、该有机物的分子式为C23H21O3NBr2 |